Die Schrödinger-Gleichung für das Wasserstoffatom
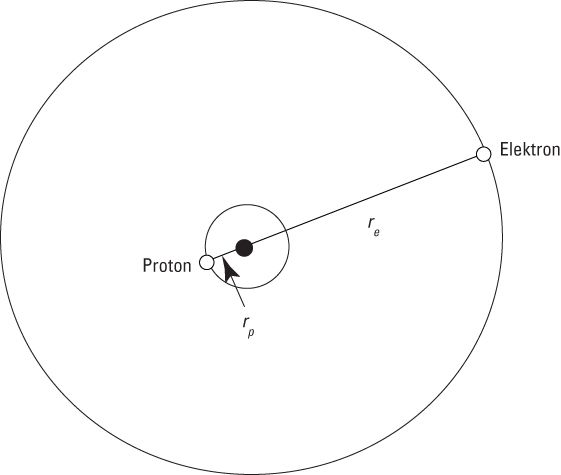
Wasserstoffatome bestehen aus einem einzelnen Proton, um das ein einzelnes Elektron kreist. Abbildung 10.1 zeigt, wie man sich das vorstellen kann.
 Beachten Sie, dass sich das Proton nicht genau
im Mittelpunkt des Atoms befindet – direkt im Mittelpunkt befindet
sich der Schwerpunkt der Massen. Vielmehr ist das Proton auf einer
Bahn mit dem Radius rp zu finden,
während sich das Elektron auf einer Bahn mit dem Radius
re um den Mittelpunkt bewegt.
Beachten Sie, dass sich das Proton nicht genau
im Mittelpunkt des Atoms befindet – direkt im Mittelpunkt befindet
sich der Schwerpunkt der Massen. Vielmehr ist das Proton auf einer
Bahn mit dem Radius rp zu finden,
während sich das Elektron auf einer Bahn mit dem Radius
re um den Mittelpunkt bewegt.
Wie lautet also die Schrödinger-Gleichung, die die benötigte Wellenfunktionen liefert? Klar, sie enthält Ausdrücke für die kinetische und die potentielle Energie von Proton und Elektron. Für die kinetische Energie des Protons gilt:

wobei  gilt. Dabei ist xp
die Position des Protons in x-Richtung, yp die in y-Richtung und zp die in z-Richtung.
gilt. Dabei ist xp
die Position des Protons in x-Richtung, yp die in y-Richtung und zp die in z-Richtung.
Die Schrödinger-Gleichung enthält auch einen Ausdruck für die kinetische Energie des Elektrons:

wobei  gilt. Dabei ist xe
die Position des Elektrons in x-Richtung, ye die in y-Richtung und ze die in z-Richtung.
gilt. Dabei ist xe
die Position des Elektrons in x-Richtung, ye die in y-Richtung und ze die in z-Richtung.
Neben der kinetischen muss man in der Schrödinger-Gleichung auch die potentielle Energie V(r) berücksichtigen. Somit lautet die zeitunabhängige Schrödinger-Gleichung:

Dabei ist ψ(re, rp) die Wellenfunktion von Elektron und Proton.
Die elektrostatische potentielle Energie V(r) für ein Zentralpotential ist durch folgende Formel gegeben, wobei r der Radiusvektor ist, der die beiden Ladungen trennt:

 In der Quantenmechanik ist es üblich, das
CGS-System (Zentimeter-Gramm-Sekunde) der Einheiten zu benutzen;
hier gilt
In der Quantenmechanik ist es üblich, das
CGS-System (Zentimeter-Gramm-Sekunde) der Einheiten zu benutzen;
hier gilt  .
.
Das von den Ladungen des Elektrons und des Protons verursachte Potential im Wasserstoffatom lautet somit:

Da r = re – rp ist, folgt für die obige Gleichung:

Damit lautet die Schrödinger-Gleichung:

Bevor die Lösung der Schrödinger-Gleichung für das Wasserstoffatom erläutert wird, wird die Gleichung im folgenden Abschnitt zunächst durch die Einführung von Relativ- und Schwerpunkt-Koordinaten vereinfacht.