7.2. Spektroskopie: Sternlicht entschlüsseln
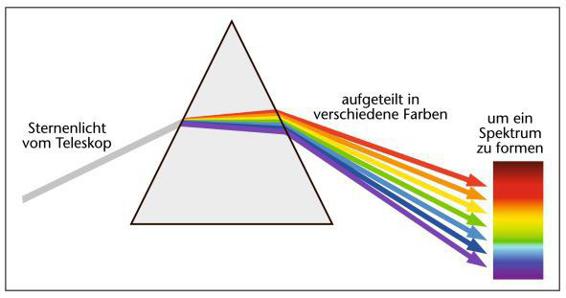
Ein Regenbogen am Himmel ist ein beeindruckendes Naturschauspiel, dessen Farbenspiel man immer wieder gerne bewundert. Bei einem solchen Ereignis wird das Sonnenlicht in kleinen Wassertröpfchen in der Atmosphäre gebrochen und reflektiert. Die verschiedenen Wellenlängen des weißen Sonnenlichts werden dabei innerhalb der vielen Tropfen auf dem Weg zu unserem Auge unterschiedlich gebrochen. Als Ergebnis sehen wir, wie sich das Licht in einem Regenbogen vor uns aufspaltet. Ein einfaches Prisma funktioniert auf die gleiche Weise. Wie in Farbabbildung 7.B schematisch dargestellt ist, werden die Wellenlängen des Lichts an der Glasfläche unterschiedlich stark gebrochen, aber nicht auch noch reflektiert. Kurzwelliges violettes Licht erfährt die stärkste Brechung, während langwelliges rotes Licht weniger stark abgelenkt wird. Das Resultat: Weißes Licht wird in seine Spektralfarben aufgespaltet.
Abb. 7.B
Diese Technik des Lichtaufbrechens machen sich Astronomen schon seit langem zunutze, indem sie das Sternlicht aufspalten und als Spektrum aufnehmen. Fraunhofer konnte so schon um 1800 Wichtiges über die Natur der Sonne erkennen. Bald darauf etablierte sich die Spektroskopie als naturwissenschaftliche Untersuchungsmethode. Parallel dazu wurden allerlei Spektrometer und Spektrographen entwickelt, die bald in jedem besseren Labor zu finden waren. In der Astronomie ermöglichte die Spektroskopie zum ersten Mal, die Physik und Chemie ferner Himmelskörper genauer zu studieren und sie trotz ihrer großen Entfernungen gewissermaßen ins Labor zu holen. Auch aus der modernen Astrophysik sind Spektrographen nicht wegzudenken. Die heutigen Apparaturen sind nur wesentlich größer als die zu Fraunhofers Zeiten, und unsere zu beobachtenden Objekte sind viel, viel weiter entfernt.
Die moderne Spektralanalyse basiert immer noch auf den gleichen Prinzipien und Erkenntnissen, die Fraunhofer eingeführt hat. Ein prominentes Beispiel sind die Fraunhofer-Linien des Kalziums, auch H und K genannt. Sie sind zwei der am stärksten ausgeprägten Linien in den meisten Sternspektren und helfen somit, sich in einem linienreichen Spektrum zu orientieren.
Aber was hat es mit den Spektrallinien grundsätzlich auf sich? Die Spektroskopie ist auch Thema in Kapitel 2.2, dort in erster Linie aber unter historischen Aspekten. Machen wir nun noch einmal einen kleinen Abstecher in die Atomphysik und betrachten, was genau mit dem Sternlicht auf dem Weg zum Spektrographen passiert. Zugunsten einer zusammenhängenden Darstellung ist die eine oder andere Wiederholung hier nicht ganz vermeidbar.
Spektroskopiert man das Licht eines glühenden, festen oder flüssigen Körpers wie z.B. eines Wolframdrahts in einer Lampe oder einer Eisenschmelze, erhält man ein sogenanntes kontinuierliches Spektrum, das sehr hübsch alle Regenbogenfarben zeigt. Ein Beispiel wird in Farbabbildung 7.C gezeigt. Ein Sternspektrum sieht bei näherem Hinsehen allerdings etwas anders aus. Wie Fraunhofer schon beobachtet hatte, befinden sich dunkle Linien in diesen Spektren. Kein Wunder, denn ein Stern mit seinen vielen Gasschichten ist komplizierter aufgebaut als ein einfacher glühender Körper. Das Licht des Sterns kommt aus dem heißen Zentrum, wo die Kernreaktionen ablaufen. Auf seinem Weg zu uns muss das Licht also durch eine dicke Schicht von kühlerem Gas in der äußeren Sternatmosphäre hindurch. Aber dies geschieht nicht ohne Verluste.
Abb. 7.C
Erinnern wir uns daran, wie ein Atom aufgebaut ist. Die positiv geladenen Atomkerne werden von negativ geladenen Elektronen umschwirrt. Im Grundzustand gibt es gleich viele Elektronen wie Protonen im Kern, so dass das Atom nach außen hin elektrisch neutral ist. Die Elektronen sausen auf verschiedenen Bahnen, die ihren Energien entsprechen. Statt von Bahnen, die im Bohr’schen Atommodell doch zu sehr an Planetenbahnen erinnern, sollte man in der Atomphysik eher von Energieniveaus sprechen. Niederenergetische Elektronen halten sich dabei meist näher am Kern auf, während sich Elektronen mit höherer Energie weiter vom Kern entfernt bewegen. Normalerweise befinden sich alle Elektronen auf Niveaus mit der niedrigstmöglichen Energie. Dies ist der Grundzustand, der für das Atom am energiesparendsten ist. Wenn aber das Licht aus dem heißen Sternzentrum die kühlere Sternatmosphäre durchstrahlt, fangen die Elektronen an, auf höhere Energieniveaus zu springen. Das kann man sich folgendermaßen vorstellen: Die Lichtteilchen – Photonen – aus dem Sterninneren haben alle möglichen Energien. Wenn ein solches Photon auf ein Atom trifft und es genügend Energie besitzt, die für einen Elektronensprung zwischen zwei Energieniveaus im Atom benötigt wird, nutzt das Elektron die Situation und springt auf das höhere Niveau. Das Photon verschwindet dabei. Jedem Elektronensprung entspricht eine ganz bestimmte Energiedifferenz und damit auch eine ganz bestimmte Lichtwellenlänge, mit der der Sprung angeregt werden kann.
Die Sprünge zwischen den Energieniveaus haben also zur Folge, dass Photonen mit ganz bestimmten Energien – Wellenlängen – aufgebraucht werden, während andere überhaupt nicht betroffen sind. Dementsprechend »fehlen« dem Sternlicht nach Durchqueren der Sternatmosphäre plötzlich bestimmte Wellenlängen. Genau dieser Effekt ist in Sternspektren beobachtbar: Die dunklen Fraunhofer-Linien sind nichts anderes als die fehlenden Wellenlängen, die das Licht sozusagen als »Zollzahlung« beim Verlassen des Sterns zurücklassen musste. Astronomen nennen diese Linien Absorptionslinien. Die Entstehung eines Absorptionslinienspektrums ist schematisch in Farbabbildung 7.C gezeigt.
Umgekehrt funktioniert es aber auch: So genannte Emissionsspektren entstehen, wenn man ein gleichmäßig heißes Gas beobachtet. Dort befinden sich alle Elektronen auf hochenergetischen Niveaus. Ab und zu springen die Elektronen auf ein niedrigeres Niveau, wobei sie die jeweilige Energie in Form eines Photons wieder abgeben. Das Licht des Gases erhält somit zusätzliche Energie bei den entsprechenden Wellenlängen. Spiralgalaxien und irreguläre Galaxien sowie Planetarische Nebel zeigen viele Emissionslinien, da sie einem riesigen Gasnebel ähneln. Die Entstehung eines Emissionslinienspektrums ist in Farbabbildung 7.C in der Mitte schematisch dargestellt.
Obwohl Gustav Kirchhoff noch nichts von den Details des Atomaufbaus und den Niveauübergängen wusste, konnte er aufgrund seiner Experimente schon um 1860 die drei Haupttypen von Spektren unterscheiden. Damit konnte er generell vorhersagen, ob ein kontinuierliches Spektrum, ein Emissionsspektrum oder ein Absorptionsspektrum bei der Beobachtung von verschiedenen Lichtquellen erwartet werden kann. Erst mit dem Bohr’schen Atommodell konnte dieses Verhalten der Spektrallinien physikalisch erklärt werden, was einen weiteren Schritt auf dem Weg zur Quantenmechanik bedeutete. Diese drei Regeln von Kirchhoff sind heute noch genauso aktuell wie vor 150 Jahren und finden besonders in der analytischen Chemie und natürlich in der Astronomie Anwendung. Sterne haben grundsätzlich Absorptionsspektren, es sei denn, sie haben eine besonders aktive Oberfläche oder sind aus irgendeinem Grund von heißem Gas umgeben, was z.B. in einem Doppelsternsystem vorkommen kann. Dann sieht man neben den Absorptionslinien zusätzlich Emissionslinien, die auf das heiße Gas zurückzuführen sind.
Mit astronomischen Beobachtungen kann man zunächst nur die äußere Hülle des Sterns untersuchen – das gilt auch für die Spektroskopie. Das Sterninnere bleibt verborgen, genauso wie man bei einem Menschen auch nur das Äußere, also die Haut, und nicht die inneren Organe sehen kann. Zum Glück gibt es verschiedene Möglichkeiten, doch noch an wichtige Informationen über das zu gelangen, was im Sterninneren vor sich geht. Nur so können Rückschlüsse auf das Sterninnere gezogen werden.
Mit Hilfe von Spektroskopie kann also etwas über die Eigenschaften des Sternatmosphärengases herausgefunden werden. Denn jedes chemische Element zeigt ein charakteristisches Linienmuster im Spektrum. Die Gesamtheit der Absorptionslinien in einem Spektrum verrät somit, welche Elemente sich in der Atmosphäre durch das Absorbieren bestimmter Wellenlängen bemerkbar gemacht haben. Die wichtigsten und oft auch stärksten Linien in einem Sternspektrum sind die Wasserstofflinien der sogenannten Balmerserie. Die stärkste dieser Linien, Hα genannt (H steht für Wasserstoff, α für die stärkste dieser Wasserstofflinien), befindet sich bei einer Wellenlänge von 656 nm im roten Spektralbereich. Die ganze Serie entsteht, wenn Elektronen vom zweiten Niveau auf weiter außen liegende Niveaus springen (siehe auch Abb. 2.3). Denn der Übergang vom zweiten zum dritten Niveau benötigt ein Photon mit der Wellenlänge von 656 nm. Viele hübsche Nebel verdanken ihre rote Farbe dem Wasserstoff und dabei besonders der Hα-Emissionslinie. Weiterhin sind die Fraunhofer’schen Kalziumlinien H und K extrem stark ausgeprägt. Sie befinden sich bei 397 und 393 nm im violetten Spektralbereich. Die Kalzium-H-Linie überlappt fast komplett mit einer der Balmerlinien, Hε. Zusätzlich können die Elemente in neutraler und ionisierter Form in der Sternatmosphäre vorkommen. Kalzium H und K gehen auf ionisiertes Kalzium zurück. Dagegen befindet sich die stärkste Linie des neutralen Kalziums bei ~422.6 nm. Drei charakteristische Magnesiumlinien um 528 nm im grünen und zwei ausgeprägte Natriumlinien bei 589 nm im gelben Bereich sind weiterhin in fast jedem Sternspektrum anzutreffen. Darüber hinaus gibt es, je nach Sterntyp, unzählige Linien von diversen anderen Elementen, also weiteren Metallen.
Zurechtfinden kann man sich in diesem Liniendschungel nur, weil die Spektren der verschiedenen Elemente ausführlich im Labor untersucht wurden. Die Angaben zu vielen tausend Spektrallinien und den atomphysikalischen Details des zugehörigen Übergangs füllen dicke Kataloge und umfangreiche Datenbanken.
Die physikalischen Bedingungen in der Sternatmosphäre sind entscheidend dafür, ob und in welcher Ausprägung eine Linie im Spektrum erscheint. So hängen die Linienstärken wesentlich von der Temperatur ab. Bei Sternen mit Oberflächentemperaturen um die 10 000 Grad Kelvin sind Wasserstofflinien am stärksten ausgeprägt. Das Umgekehrte gilt für Metalllinien, die so schwach geworden sind, dass sie kaum mehr im Spektrum anzufinden sind. Allerdings tauchen in Spektren von Sternen mit mindestens 10 000 Grad Oberflächentemperatur dafür Heliumlinien auf. Bei kühleren Sternen reicht die Lichtenergie nicht aus, um die Elektronen der Heliumatome in höhere Niveaus zu stupsen. Bei kühleren Sternen wie der Sonne, die ein 5500 Grad C heißer Hauptreihenstern ist, sind die Balmerlinien ebenfalls schwächer, aber immer noch dominant im Spektrum vertreten. Die Metalllinien sind deutlich ausgeprägt. Dieses Verhalten ist in Abbildung 7.3 gezeigt. Kühle Rote Riesen haben wiederum schmalere Wasserstofflinien, aber dafür stärker ausgeprägte Metalllinien. Bei noch viel kühleren Sternen, z.B. mit nur 2000 Grad Kelvin, finden sich schließlich sogar Bänder von unzähligen übereinanderlappenden Titanoxidlinien im Spektrum, da die niedrige Temperatur die Bildung von Molekülen in der Sternatmosphäre zulässt.
Abb. 7.3 : Normalisierte Spektren zweier verschieden heißer Sterne mit gleicher Metallizität. Die Linienstärken sind trotz gleicher Metallhäufigkeiten unterschiedlich. Das obere Spektrum ist für eine bessere Ansicht nach oben versetzt.
Jedes Spektrum ist somit der »Fingerabdruck« des Sterns, anhand dessen man auf seine Natur und seine Eigenschaften schließen kann. Schon vor 1900 wurden die ersten sogenannten Spektralklassen eingeführt, um eine systematische Ordnung in die Vielfalt der Spektren zu bringen. Bald darauf wurde die verfeinerte O B A F G K M-Sequenz mit zusätzlichen Nummerierungen für Untergruppen vorgeschlagen. Zur gleichen Zeit wurden Tausende von Sternen durch Annie Jump Cannon klassifiziert (siehe auch Kapitel 2.3). Es stellte sich heraus, dass die Spektralklassen mit den unterschiedlichen Linienstärken im Wesentlichen eine Temperatursequenz darstellen. Die noch heute benutzten Spektralklassen und die dazugehörigen Sterntemperaturen sind in Tabelle 7.1 aufgelistet. Sterne des O-Typs haben eine Oberflächentemperatur von 40 000 Grad Kelvin. M-Sterne sind dagegen weniger als 3000 Grad Kelvin »kühl«.
Tabelle 7.1 : Zusammenhang zwischen Spektraltyp und Temperatur.
Spektraltyp |
Farbe |
Temperatur (in Grad K) |
O |
Blau |
30000 – 50000 |
B |
Blau, blau-weißlich |
10000 – 3000 |
A |
Weiß |
7500 – 10000 |
F |
Gelb-weißlich |
6000 – 7000 |
G |
Gelb |
4500 – 6000 |
K |
Rötlich-orange |
3500 – 4500 |
M |
Rot |
2000 – 3000 |
Moderne Spektralanalysen haben gezeigt, dass die meisten Sterne eine Vielfalt von Elementen in ihren Atmosphären aufweisen und dass ihre Metallizität der der Sonne sehr ähnlich ist. Dennoch gibt es auch metallarme Sterne, die geringere Metallizitäten als die Sonne besitzen. Wie sehen dann die Spektren von Sternen mit unterschiedlichen Metallizitäten aus? Betrachtet man zwei gleich heiße Sterne, einen so metallreich wie die Sonne und einen hundertmal metallärmeren, wird der Unterschied sofort deutlich: Der metallarme Stern hat wesentlich schwächere Linien, wie in Abbildung 7.4 gesehen werden kann. Da die Konzentration der Elemente in der Atmosphäre in metallarmen Sternen geringer ist, sind weniger Atome dieser Elemente vorhanden, die bei den für die Energieniveaus im Atom charakteristischen Wellenlängen Licht absorbieren würden. Umgekehrt haben heißere Sterne bei gleicher Metallizität schwächere Absorptionslinien als kühlere Sterne. Wenn wir also metallarme Sterne finden wollen, müssen wir nach Sternen suchen, die besonders bei kühleren Temperaturen sehr schwache Metalllinien zeigen.
Abb. 7.4: Spektren mit ähnlichen Temperaturen, aber unterschiedlichen Metallizitäten. Oben: die metallreiche Sonne mit [Fe/H] = 0. Mitte: zwei Sterne mit niedrigeren Metallizitäten. Unten: der eisenärmste Stern mit [Fe/H] = –5,4. Die Bedeutung von »[Fe/H]« wird in Kapitel 7.3 beschrieben. Alle Spektren sind normalisiert und versetzt gezeigt.