«És com l’anguila, d’esmunyedís»
Amb la molècula proteica, la Naturalesa ha creat un instrument en què una simplicitat subjacent serveix per expressar una gran subtilesa i versatilitat; no es pot apreciar la biologia molecular en tot el seu abast fins que no es percep clarament aquesta peculiar combinació de qualitats.
FRANCIS CRICK
Abans he escrit que el terme codi procedeix de caudex, el cor llenyós de l’arbre que es feia servir per redactar manuscrits antics. És seductor pensar que un material utilitzat per escriure-hi un codi engendrés la paraula mateixa: la forma convertida en funció. També en el cas de l’ADN, com Watson i Crick van veure, la forma de la molècula havia d’estar relacionada intrínsecament amb la funció. El codi genètic havia d’estar escrit al material que constituïa l’ADN d’una manera tan íntima com les lletres quedaven gravades al còdex.
¿Què era, però, el codi genètic? ¿Com podia ser que quatre bases d’una cadena molecular d’ADN —A, C, G i T (o A, C, G i U a l’ARN)— determinessin la consistència dels cabells, el color dels ulls o el tipus de revestiment d’un bacteri (o bé la propensió a patir un trastorn mental o una malaltia hemorràgica mortal d’origen hereditari)? ¿Com es manifestava la «unitat hereditària» abstracta de Mendel en forma de característica física?
* * *
El 1941, tres anys abans del crucial experiment d’Avery, dos científics, George Beadle i Edward Tatum, mentre investigaven en un corredor subterrani de la universitat californiana d’Stanford, van descobrir el vincle que faltava entre els gens i els trets físics. Beadle —en «Beet», com n’hi deien els companys— havia sigut alumne de Thomas Morgan al California Institute of Technology. Les mosques d’ulls vermells i les mosques mutants d’ulls blancs el desconcertaven. El «gen de la vermellor», segons Beadle, és una unitat d’informació hereditària, i es transmet de pares a fills en una forma indivisible d’ADN: en forma de gens, de cromosomes. La «vermellor» com a tret físic, en canvi, era conseqüència d’un pigment químic de l’ull. Ara bé, ¿com es transmutava una partícula hereditària en un pigment ocular? ¿Quin era el lligam entre el «gen de la vermellor» i la «vermellor» pròpiament dita, és a dir, entre la informació i la manifestació material o anatòmica?
La mosca del vinagre havia transformat la genètica per obra d’uns mutants poc freqüents. Era precisament per la seva poca freqüència que els mutants havien actuat com uns fars enmig de la foscor que havien permès als biòlegs rastrejar «l’acció d’un gen», com Morgan ho havia definit, al llarg de les generacions. Però «l’acció» d’un gen continuava sent una noció vaga i misteriosa, i intrigava Beadle. A finals de la dècada del 1930, Beadle i Tatum van pensar que aïllar el pigment ocular de la mosca del vinagre podia resoldre l’enigma de l’acció gènica. L’estudi, però, va quedar aturat perquè la relació entre els gens i els pigments era massa complexa per sustentar una hipòtesi plausible. L’any 1937, a la universitat d’Stanford, Beadle i Tatum van centrar-se en un organisme encara més simple, Neurospora crassa, una floridura del pa que havia aparegut com a contaminant en una fleca francesa, per mirar de descobrir la relació entre gen i caràcter.
Les floridures del pa són uns organismes primitius i voraços. Es poden cultivar en plaques de Petri amb un brou de cultiu ric en nutrients, però de fet no necessiten gaire cosa per viure. Eliminant progressivament quasi tots els nutrients del brou, Beadle va descobrir que les soques de floridura eren capaces de continuar desenvolupant-se en un brou mínim que contenia únicament un sucre i una vitamina anomenada biotina. Les cèl·lules de la floridura, de forma natural, eren capaces de sintetitzar totes les molècules que necessitaven per sobreviure a partir de substàncies químiques bàsiques; és a dir, lípids a partir de la glucosa, ADN i ARN a partir de substàncies precursores, i carbohidrats complexos a partir de sucres simples. El miracle del pa.
Beadle va considerar que aquesta capacitat es devia a la presència d’enzims cel·lulars, unes proteïnes que feien de mestre d’obres i podien sintetitzar complexes macromolècules biològiques a partir de substàncies químiques precursores bàsiques. Perquè una floridura del pa creixés bé en un medi mínim, doncs, necessitava conservar intactes totes les seves funcions metabòliques de fabricació de molècules. Si alguna mutació inactivava ni que fos una sola funció, la floridura perdia la facultat de créixer, si no era que al brou s’hi afegia el component que li faltava. Beadle i Tatum van poder utilitzar aquesta tècnica per descobrir quina era la funció metabòlica absent en cada mutant. Si un mutant necessitava la substància X per créixer en un medi mínim, per exemple, significava que li devia faltar l’enzim que sintetitzava aquella substància X a partir de zero. Es tractava d’una tècnica molt laboriosa, però la paciència era una virtut que Beadle tenia en abundància: una vegada s’havia passat tota una tarda ensenyant a un estudiant de doctorat a condimentar un bistec afegint-hi les espècies una per una a intervals de temps regulars.
L’experiment del «component absent» va conduir Beadle i Tatum a veure els gens des d’una òptica nova. Van observar que a cada mutant li faltava una única funció metabòlica, que corresponia a l’activitat d’un únic enzim proteic. I els encreuaments genètics van revelar que cada mutant estava mancat d’un únic gen.
Si una mutació impedeix la funció d’un enzim, doncs, el gen normal ha d’especificar la informació per fabricar l’enzim normal. Una unitat hereditària ha de contenir el codi per portar a terme un funció metabòlica o cel·lular especificada per una proteïna. «Un gen», va escriure Beadle el 1945, «es pot imaginar com el responsable de la configuració final d’una molècula proteica». Aquesta era l’«acció del gen» que tota una generació de biòlegs havia estat intentant comprendre: un gen «actua» per mitjà de la informació codificada que conté per fabricar una proteïna, i la proteïna actualitza la forma o la funció de l’organisme.[027]
Representat en termes de flux d’informació:
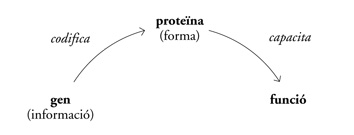
El 1958 Beadle i Tatum van compartir un premi Nobel per aquest descobriment, però l’experiment Beadle/Tatum va suscitar una pregunta cabdal que va quedar sense resposta: ¿com «conté» un gen la informació necessària per fabricar una proteïna? Una proteïna se sintetitza a partir de vint substàncies químiques més simples anomenades aminoàcids —metionina, glicina, leucina, etcètera— unides en forma de cadena. A diferència de la cadena d’ADN, que a la naturalesa existeix majoritàriament en forma de doble hèlix, una cadena de proteïna té la capacitat de recargolar-se a l’espai de manera característica i singular, com un filferro entortolligat. Aquesta facultat d’adquirir una forma concreta permet a les proteïnes de complir diverses funcions cel·lulars. Poden existir com a fibres llargues i elàstiques als músculs (com la miosina); poden prendre una forma globular i facilitar reaccions químiques com en el cas dels enzims (com la polimerasa d’ADN); poden enllaçar-se amb substàncies químiques acolorides i convertir-se en pigments oculars o florals; plegades com un tancador, poden fer de vehicle transportador d’altres molècules (com l’hemoglobina); poden especificar la manera com una cèl·lula nerviosa es comunica amb una altra cèl·lula nerviosa i, per tant, erigir-se en àrbitres de la cognició normal i del desenvolupament neuronal.
Ara bé, ¿com pot una seqüència d’ADN —ATGCCCC…, etc.— contenir les instruccions per fabricar una proteïna? Watson havia sospitat sempre que l’ADN es convertia prèviament en un missatge intermedi. Era aquesta «molècula missatgera», com ell en deia, la que contenia les instruccions per fabricar una proteïna a partir d’un gen «Al llarg de més d’un any», va escriure el 1953, «havia estat dient a en Francis [Crick] que la informació genètica de les cadenes d’ADN s’havia de copiar primer en forma de molècules complementàries d’ARN», i que les molècules d’ARN devien fer de «missatger» a l’hora de fabricar proteïnes.
El 1954, el físic d’origen rus George Gamow, reconvertit en biòleg, va formar amb Watson un «club» de científics per desxifrar el mecanisme de la síntesi proteica. «Benvolgut Pauling», va escriure Gamow a Linus Pauling el 1954, amb la seva característica interpretació liberal de la gramàtica i la redacció angleses, «estic entretingut amb molècules orgàniques complexes (una cosa que no havia fet mai!) i he obtingut uns quants resultats interessants que m’agradaria que me’n donessis l’opinió».
Gamow va batejar el grup amb el nom de RNA Tie Club («el Club de la Corbata d’ARN»). «El club no es va arribar a reunir mai en ple», recordava Crick; «sempre va tenir una existència bastant etèria». No hi havia reunions formals, ni normes, ni tan sols uns principis organitzatius bàsics. El Tie Club, més aviat, existia només en forma de trobades i converses informals. Les reunions es feien improvisadament, o ni tan sols es feien. Entre els membres del club s’enviaven cartes en què postulaven hipòtesis esbojarrades i inèdites, sovint acompanyades d’esbossos dibuixats a mà; era una mena de blog anterior als blogs. Watson va encomanar en una camiseria de Los Angeles que els fes unes corbates de llana verda amb el brodat d’una cadena d’ARN de color daurat, i Gamow va enviar una corbata amb una agulla a cada membre de la colla d’amics que havia triat com a integrants del club. Va fer imprimir paper de carta amb un membret i hi va afegir una divisa: «A totes o res». («Do or die, or don’t try»).
* * *
A mitjans de la dècada del 1950, dos genetistes bacterians que treballaven a París, Jacques Monod i François Jacob, també havien realitzat uns quants experiments que suggerien vagament que calia una molècula intermediària —o missatgera— per produir proteïnes a partir de l’ADN. Postulaven que els gens no transmetien directament les instruccions per fer proteïnes, sinó que la informació genètica de l’ADN es transformava primer en una mena de còpia escanejada —una versió transitòria—, i que era aquesta còpia, i no l’ADN original, el que es traduïa a proteïna.
L’abril del 1960, Crick i Jacob es van trobar al pis petit com un cop de puny que Sydney Brenner tenia a Cambridge per debatre sobre la identitat d’aquell intermediari misteriós. Brenner, fill d’un sabater sud-africà, havia anat a Anglaterra a estudiar biologia amb una beca; igual que Watson i Crick, també havia quedat seduït per l’ADN i la «religió dels gens» iniciada per Watson. Mentre encara estaven paint el dinar, els tres científics van deduir que la seva molècula intermediària havia de desplaçar-se del nucli de la cèl·lula, que era on estaven els gens, al citoplasma, que era on se sintetitzaven les proteïnes.
Ara bé, ¿quina era la identitat química del «missatger» que es fabricava a partir del gen? ¿Era una proteïna, un àcid nucleic o alguna altra mena de molècula? ¿Quina relació tenia amb la seqüència gènica? Tot i que encara no disposaven de proves empíriques, tant Brenner com Crick també sospitaven que es tractava d’ARN, el cosí molecular de l’ADN. El 1959, Crick va escriure per al Tie Club un poema que no va arribar a enviar:
¿Quines propietats té l’ARN genètic?
¿És al cel o és al paradís?
És com l’anguila, d’esmunyedís.
* * *
Al començament de la primavera del 1960, Jacob va agafar l’avió per anar al California Institute of Technology a treballar amb Matthew Meselson i mirar d’atrapar aquella «anguila». Brenner hi va arribar al cap de poques setmanes, a primers de juny.
Tant Brenner com Jacob sabien que les proteïnes se sintetitzaven a l’interior de la cèl·lula per mitjà d’un element cel·lular especialitzat que es deia ribosoma. La manera més segura d’obtenir el missatger intermediari era interrompre de cop la síntesi proteica —per mitjà de l’equivalent bioquímic d’una dutxa freda— i separar les esquives molècules associades amb els ribosomes per atrapar l’anguila.
El principi semblava clar, però l’experiment pròpiament dit va resultar ser misteriosament inaccessible. Brenner va escriure que, al principi, l’única cosa que va veure a l’experiment va ser l’equivalent d’una espessa «boira californiana: humida, freda i silenciosa». S’havien passat setmanes preparant la seva complicada trampa bioquímica; però, cada vegada que atrapaven els ribosomes, es degradaven i es desfeien. A l’interior de la cèl·lula, els ribosomes es mantenien cohesionats amb una normalitat absoluta. ¿Per què fora de la cèl·lula es desagregaven, com una boira que se’ls esmunyís entre els dits?
La resposta va sorgir de la boira mateixa. Un matí que Brenner i Jacob eren a la platja, Brenner, mentre cavil·lava sobre les seves classes de bioquímica bàsica, va prendre consciència d’un fet ben simple: que a les seves solucions devia faltar-hi algun factor químic essencial que mantenia els ribosomes intactes a l’interior de les cèl·lules. Però ¿quin factor? Havia de ser una cosa petita, comuna i ubiqua; una goteta molecular adhesiva. De cop es va aixecar de la sorra d’una revolada, amb els cabells voleiant-li i la sorra caient-li de les butxaques, cridant: «És el magnesi! És el magnesi!».
Era el magnesi. L’addició d’aquest ió va ser definitiva: amb la solució enriquida amb magnesi, els ribosomes es van mantenir cohesionats, i Brenner i Jacob van poder obtenir per fi una quantitat molt petita de la molècula missatgera de la cèl·lula bacteriana. Era ARN, tal com esperaven, però un ARN d’un tipus especial.[028] El missatger se sintetitzava de nou en nou cada vegada que s’havia de traduir un gen. Igual que l’ADN, aquestes molècules d’ARN estaven formades per mitjà de l’encadenament de quatre bases: A, G, C i U (recordem que, a la còpia d’ARN d’un gen, les T de l’ADN són reemplaçades per U). Temps més tard Brenner i Jacob van descobrir que, més concretament, l’ARN missatger era un «facsímil» de la cadena d’ADN, és a dir, una còpia de l’original. La còpia d’ARN del gen passava tot seguit del nucli al citosol, on el missatge era descodificat per fabricar la proteïna corresponent. L’ARN missatger no vivia ni a l’infern ni al paradís, sinó que era un mitjancer professional. La generació de la còpia d’ARN d’un gen va rebre el nom de transcripció, amb el sentit de reescriptura d’un mot o una locució en una llengua pròxima a l’original. El codi d’un gen (ATGGGCC…) es transcrivia en el codi de l’ARN (AUGGGCC…).
El sistema era semblant al fet d’anar a una biblioteca de llibres rars a fer-hi una traducció. L’original amb la informació —és a dir, el gen— estava guardat permanentment en una mena de magatzem blindat o cambra cuirassada. Quan la cèl·lula feia una «sol·licitud de traducció», des de la cambra del nucli se li subministrava una còpia de l’original. Aquest facsímil d’un gen (és a dir, l’ARN) s’utilitzava com a font operativa de traducció per obtenir la proteïna corresponent. Aquest sistema permetia que hi pogués haver en circulació moltes còpies d’un sol gen a la vegada, i que les còpies d’ARN augmentessin o disminuïssin a discreció; uns fets que, com no trigaria a demostrar-se, eren essencials per comprendre l’activitat i la funció dels gens.
* * *
La transcripció, però, tan sols resolia la meitat del problema de la síntesi proteica. Quedava per resoldre l’altra meitat: ¿Com es descodificava el «missatge» de l’ARN per obtenir una proteïna? Per fer una còpia d’ARN d’un gen, la cèl·lula recorria a una transcripció bastant senzilla: els A, C, T i G del gen es copiaven en forma d’A, C, U i G en l’ARN missatger (és a dir, ACT CCT GGG → ACU CCU GGG). L’única diferència en el codi entre l’original del gen i la còpia de l’ARN era la substitució de la timina per un uracil (T → U). Un cop feta la transcripció a ARN, però, ¿com es descodificava el «missatge» d’un gen per obtenir-ne la proteïna corresponent?
Per Watson i Crick, era ben clar que una base tota sola —A, C, T o G– no podia contenir un missatge genètic suficient per sintetitzar cap component proteic. En total hi ha vint aminoàcids, i quatre lletres totes soles no podien representar vint estats alternatius. La resposta havia d’estar en la combinació de les bases. «Sembla probable», van escriure, «que la seqüència precisa de les bases sigui el codi que conté la informació genètica».
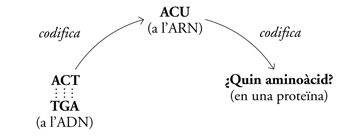
Per il·lustrar-ho pot servir una analogia amb el llenguatge humà. Les lletres A, C i T contenen molt poc significat independentment, però es poden combinar per tal de crear missatges substancialment diferents. Novament és la «seqüència» el que conté el missatge: amb aquestes tres lletres es poden formar, per exemple, tres paraules angleses —act, tac i cat— de significats completament diferents. La clau per descobrir el codi genètic era fer correspondre els elements d’una seqüència d’una cadena d’ARN a la seqüència de la cadena proteica corresponent. Era com desxifrar la pedra Rosetta de la genètica: ¿quina combinació de lletres (de l’ARN) representava la combinació corresponent de lletres (de la proteïna)? O, conceptualment:
Per mitjà d’una sèrie d’experiments enginyosos, Crick i Brenner van deduir que el codi genètic havia d’operar en forma de «triplets»; és a dir, que tres bases d’ADN (ACT, per exemple) havien de representar un aminoàcid d’una proteïna.[029]
Ara bé, ¿quin triplet representava quin aminoàcid? Pels volts del 1961, uns quants laboratoris d’arreu del món s’havien afegit a la cursa per desxifrar el codi genètic. Als National Institutes of Health de Bethesda, Marshall Nirenberg, Heinrich Matthaei i Philip Leder van intentar desxifrar-lo des de l’àmbit de la bioquímica. Un químic originari de l’Índia, Har Khorana, va obtenir reactius químics essencials per fer possible el desxiframent del codi. I un bioquímic espanyol establert a Nova York, Severo Ochoa, va iniciar una tasca paral·lela per relacionar el codi de triplets amb els diferents aminoàcids.
Com en qualsevol procés de desxiframent, els avenços es van anar fent a còpia d’errors. Al principi va semblar que els triplets se solapaven l’un a l’altre, possibilitat que impedia l’existència d’un codi senzill. Posteriorment, durant un temps, va semblar que hi havia triplets que no complien cap mena de funció. El 1965, però, tots aquests estudis —especialment el de Nirenberg— havien aconseguit relacionar cada triplet d’ADN amb un aminoàcid concret. ACT, per exemple, corresponia a l’aminoàcid treonina. CAT, en canvi, en representava un de diferent, la histidina. CGT corresponia a l’arginina. Una seqüència concreta d’ADN —ACT-GAC-CAC-GTG— servia per construir una cadena d’ARN, i la cadena d’ARN era traduïda en forma de cadena d’aminoàcids, cosa que conduïa a l’obtenció d’una proteïna. El triplet ATG era el codi per iniciar la síntesi d’una proteïna, mentre que n’hi havia tres (TAA, TAG i TGA) que donaven l’ordre d’aturar-la. L’alfabet bàsic del codi genètic s’havia descobert.
La transmissió de la informació es pot representar de forma ben senzilla:
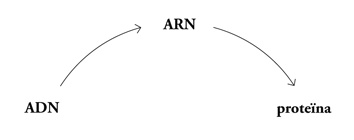
O, conceptualment:

O bé:

Francis Crick va anomenar aquesta transmissió d’informació «el dogma central» de la informació biològica. El terme dogma va ser una tria capritxosa (més tard Crick va reconèixer que no havia arribat a entendre mai el contingut conceptual de dogma, que va associat a una convicció fixa i immutable), però el qualificatiu de central va ser encertat. Crick feia referència a la colpidora universalitat de la transmissió de la informació genètica en el món dels éssers vius.[030] Des dels bacteris fins als elefants, des de les mosques d’ulls vermells fins als prínceps de sang blava, la informació biològica es transmetia d’un organisme viu a un altre d’una manera sistemàtica i arquetípica: l’ADN donava les instruccions per fabricar l’ARN; l’ARN donava les instruccions per fabricar les proteïnes; i les proteïnes, manifestació viva dels gens, formaven les estructures i complien les funcions que se’ls havien transmès.
* * *
Una de les malalties que segurament il·lustra de manera més contundent aquesta transmissió de la informació i els seus efectes palpables en la fisiologia humana és l’anèmia falciforme o drepanocitosi. Ja al segle VI abans de Crist, els metges aiurvèdics de l’Índia havien reconegut els símptomes generals de l’anèmia —o absència de glòbuls vermells normals a la sang— en forma d’una pal·lidesa característica dels llavis, la pell i els dits de les mans. Les anèmies, conegudes en sànscrit amb el nom de pandu roga, es dividien en diferents categories. Se sabia que algunes variants de la malaltia eren degudes a la malnutrició, i es creia que algunes altres eren provocades per episodis hemorràgics. L’anèmia falciforme, però, devia semblar la més estranya, perquè era hereditària i anava acompanyada sovint de crisis i espasmes i de sobtats atacs lancinants de dolor als ossos, les articulacions i el pit. La tribu ga de l’Àfrica occidental donava a aquest dolor el nom de chwechweechwe (‘rosecs’). Els ewe en deien nuiduidui (‘torçons’), termes onomatopeics amb una sonoritat que sembla voler copsar el caràcter implacable d’un dolor en què sembla que et perforin el moll de l’os amb barrines.
El 1904, una imatge vista a través del microscopi va revelar quina era la causa que explicava tots aquells símptomes sense relació aparent. Aquell any, un jove estudiant d’odontologia que es deia Walter Noel va anar a visitar-se a Chicago amb el seu metge perquè tenia una crisi aguda d’anèmia acompanyada del dolor ossi i toràcic característic. Noel era caribeny, originari de l’Àfrica occidental, i havia patit uns quants episodis semblants al llarg dels anys anteriors. El cardiòleg, James Herrick, va descartar que pogués ser un atac de cor, i, sense donar-hi més importància, va derivar el cas a un metge intern resident que es deia Ernest Irons. I a Irons se li va acudir d’examinar la sang de Noel al microscopi.
Irons va descobrir-hi una alteració desconcertant. Els glòbuls vermells normals tenen forma de disc aplanat, una forma que els permet apilar-se l’un sobre l’altre i per tant desplaçar-se de forma fluida per les xarxes d’artèries, capil·lars i venes per fer arribar l’oxigen al fetge, el cor i el cervell. A la sang de Noel, però, els glòbuls vermells s’havien transformat, misteriosament, en una mena de mitges llunes pansides, amb forma de falç; «cèl·lules falciformes», tal com Irons les va descriure més tard.
Ara bé, ¿què feia que un glòbul vermell agafés forma de falç? I ¿per què era una malaltia hereditària? El culpable últim era una anomalia en el gen de l’hemoglobina (la proteïna que transporta l’oxigen i és molt abundant en els glòbuls vermells). El 1951, mentre treballava amb Harvey Itano al California Institute of Technology, Linus Pauling va demostrar que la variant d’hemoglobina que contenien les cèl·lules falciformes era diferent que l’hemoglobina dels glòbuls normals. Cinc anys més tard, uns investigadors de Cambridge van atribuir la diferència entre la cadena proteica d’hemoglobina normal i la d’hemoglobina «falciforme» a un canvi d’un sol aminoàcid.[031]
Ara bé, si la cadena proteica tenia canviat un sol aminoàcid, el gen que li corresponia havia de diferir del gen normal en un sol triplet («un triplet codifica un aminoàcid»). Doncs bé: tal com s’havia anticipat, quan temps més tard es va identificar i seqüenciar la cadena d’hemoglobina B en pacients amb cèl·lules falciformes, s’hi va trobar un sol canvi: un triplet de l’ADN (GAG) estava canviat per un altre (GTG). Això comportava la substitució d’un aminoàcid per un altre: en lloc de glutamat hi havia valina. Aquest canvi alterava el plegament de la cadena d’hemoglobina: en comptes de cargolar-se per formar la seva estructura de tancador perfectament articulada, la proteïna d’hemoglobina mutant s’acumulava a l’interior dels glòbuls vermells en forma d’agregats filamentosos. Aquests agregats s’arribaven a fer tan grossos, sobretot en absència d’oxigen, que tibaven la membrana del glòbul vermell i deformaven la seva estructura normal de disc fins a convertir-lo en una «cèl·lula falciforme», és a dir, amb forma de falç o de mitja lluna. Incapaces de lliscar amb fluïdesa pels capil·lars i les venes, les cèl·lules falciformes formaven grumolls microscòpics per tot el cos, interrompien la circulació de la sang i provocaven el dolor atroç d’una crisi drepanocítica.
Era una malaltia de «reacció en cadena»: un canvi en la seqüència d’un gen causava un canvi en la seqüència d’una proteïna, cosa que feia que agafés una forma torta, cosa que causava que els glòbuls s’arronsessin, cosa que obstruïa una vena, cosa que interrompia la circulació, cosa que feia patir el cos (que els gens havien construït). Gen, proteïna, funció i destí anaven encadenats; amb una alteració química en un parell de bases de l’ADN n’hi havia prou per «codificar» un canvi radical en el destí de la persona.