4. ¿De qué están hechas las cosas?

EN LA ÉPOCA VICTORIANA, uno de los libros favoritos de los niños británicos era Book of Nonsense (Libro de sinsentidos), de Edward Lear. Además de The Owl and the Pussycat (poemas sobre un búho y un gato que quizá conozcas porque aún son famosos), The Jumblies (unos personajes coloridos y llenos de aventura) y The Pobble Who Has No Toes (el «Pobble» que perdió los dedos), me encantan las recetas que aparecen al final del libro. La de los Crumboblious (palabra inventada por el autor) comienza así:
Consigue algunas tiras de carne; córtalas en los pedazos más pequeños posibles; y procede después a cortarlos en pedacitos aún más pequeños; ocho o quizá nueve veces más.
¿Qué obtenemos si seguimos cortando algo en pedazos cada vez más pequeños?
Supón que coges cualquier cosa y la cortas por la mitad, utilizando para ello la cuchilla de afeitar más fina y afilada que puedas encontrar.
Después cortas cada mitad por la mitad, y de nuevo por la mitad, y así una y otra vez.
¿Llegarán los trozos a ser tan pequeños que ya no puedan ser más pequeños? ¿Cómo de fino es el filo de una cuchilla de afeitar? ¿De qué tamaño es la punta de un alfiler?
¿Cuáles son las unidades más pequeñas en las que se puede dividir una cosa?
Las civilizaciones antiguas de Grecia, China e India creían haber llegado a la misma conclusión, que todo estaba hecho de cuatro «elementos»: aire, agua, fuego y tierra.
Pero un griego antiguo llamado Demócrito se acercó un poco más a la verdad. Demócrito pensó que si cortamos algo hasta el punto de conseguir trozos lo suficientemente pequeños, llegará un momento en que ya no se podrá cortar más. La palabra griega para «cortar» es tomos, y el prefijo «a» significa «no» o «no se puede» Por tanto, «atómico» significa algo tan pequeño que no se puede dividir en trozos más pequeños, y de ahí procede la palabra «átomo». Un átomo de oro es el trozo de oro más pequeño que puede existir. Incluso si pudiera cortarse en trozos más pequeños, dejaría de ser oro. Un átomo de hierro es el trozo de hierro más pequeño que puede existir. Y así con todo.
Ahora sabemos que existen unos 1000 tipos de átomos diferentes, de los que solo un 90 por ciento se encuentran en la naturaleza. El resto han sido creados en laboratorios científicos, pero solo en cantidades mínimas.

Las sustancias puras que están compuestas únicamente por un tipo de átomo se denominan elementos (la misma palabra que una vez se utilizó para la tierra, el agua, el aire y el fuego, pero con un significado muy diferente) Algunos ejemplos de elementos son el hidrógeno, el oxígeno, el hierro, el cloro, el cobre, el sodio, el oro, el mercurio y el nitrógeno. Algunos elementos, como el molibdeno, son muy escasos en la Tierra (quizá por eso nunca hayas oído hablar del molibdeno), pero muy abundantes en otras partes del universo (si te estás preguntando cómo lo sabemos, espera al Capítulo 8).
Metales como el hierro, el plomo, el cobre, el cinc, el estaño y el mercurio son elementos. También lo son algunos gases como el oxígeno, el hidrógeno, el nitrógeno y el neón. Pero la mayoría de las sustancias que nos rodean no son elementos, sino compuestos. Un compuesto es lo que obtenemos cuando dos o más átomos diferentes se unen de una forma concreta. Probablemente hayas oído hablar del agua como «H2O». Se trata de una fórmula química, y significa que es un compuesto formado por un átomo de oxígeno unido a dos átomos de hidrógeno. Los grupos de átomos se unen para formar un compuesto llamado molécula. Algunas moléculas son muy simples: una molécula de agua, por ejemplo, solo tiene esos tres átomos. Otras moléculas, sobre todo las que se encuentran en los cuerpos vivos, tienen cientos de átomos, todos unidos en una estructura muy particular. De hecho, es esa forma de unirse entre ellos, además del tipo y el número de átomos, lo que hace que una molécula en particular sea un compuesto y no otro.

También puedes utilizar la palabra «molécula» para describir lo que se obtiene cuando se unen dos o más átomos del mismo tipo. Una molécula de oxígeno, ese gas que necesitamos para respirar, está compuesta por dos átomos de oxígeno unidos. A veces se unen tres átomos de oxígeno para dar lugar a un tipo de molécula diferente llamada ozono. Es el número de átomos en una molécula lo que marca realmente la diferencia, incluso si los átomos son iguales.
El ozono es dañino si se respira, pero nos beneficiamos de la capa que forma en la atmósfera superior de la Tierra, que nos protege de los rayos más dañinos del sol. Uno de los motivos por los que los australianos toman tantas precauciones cuando se exponen al sol es que existe un «agujero» en la parte más al sur de la capa de ozono.

Cristales, un desfile de átomos
Un cristal de diamante es una molécula enorme sin tamaño fijo, formada por millones de átomos del elemento carbono pegados entre sí, todos alineados de una forma muy concreta. Están organizados de tal modo dentro del cristal que podrían parecer los soldados de un desfile, salvo que en este caso el desfile es en tres dimensiones, como un banco de peces. Pero el número de peces en el banco —el número de átomos de carbono en el cristal de diamante más pequeño— es gigantesco, más que todos los peces (y todas las personas) del mundo. Y «pegados» es un término erróneo para describirlos si con eso damos a entender que los átomos son pedazos de carbono tan juntos que no hay espacio entre ellos. De hecho, tal como veremos, la mayoría de la materia sólida está formada por espacio vacío. ¡Eso hará falta explicarlo! Enseguida volvemos con ello.
Todos los cristales están construidos con la misma forma a de «desfile de soldados», con átomos espaciados regularmente en un patrón fijo que es el que da a al cristal su forma. De hecho, eso es lo que significa cristal. Algunos «soldados» son capaces de desfilar de más de una forma, produciendo cristales muy diferentes. Los átomos de carbono, si desfilan de una forma, crean el legendario y duro cristal de diamante. Pero si adoptan una formación diferente construyen cristales de grafito, tan suave que se utiliza como lubricante.
Pensamos en los cristales como objetos maravillosos y transparentes, e incluso describimos otras cosas como el agua pura diciendo que es de una «claridad cristalina». Pero en realidad, la mayoría de la materia sólida está hecha de cristales, y la mayoría de la materia sólida no es transparente. Un trozo de hierro está hecho de multitud de pequeños cristales empaquetados, cada uno de ellos formado por millones de átomos de hierro, ordenados en formación, igual que los átomos de carbono en el cristal de diamante. El plomo, el aluminio, el oro, el cobre: todos están hechos de cristales de sus distintos tipos de átomos. También las rocas, como el granito o la arenisca, pero estas suelen ser mezclas de muchos tipos diferentes de pequeños cristales todos empaquetados juntos.

La arena también es cristalina. De hecho, muchos granos de arena son como pequeñas rocas erosionadas por el agua y el viento. Y el barro, aunque con el añadido de agua u otros líquidos. A menudo, los granos de arena se unen con granos de barro para formar nuevas rocas, denominadas «sedimentarias» porque están formadas por sedimentos endurecidos de arena y barro. (Un «sedimento» es la parte sólida que queda a en el fondo de un líquido, por ejemplo, en un río, un lago o el mar). La arena de las rocas areniscas está hecha principalmente de cuarzo y feldespato, dos cristales comunes en la corteza terrestre. La piedra caliza es diferente. Igual que la tiza es carbonato de calcio, y procede de los esqueletos de los corales y de las conchas, incluyendo las conchas de pequeñas criaturas de una única célula llamadas foraminíferos. Si ves una playa muy blanca, probablemente la arena será en su mayor parte calcio carbonatado del mismo tipo de concha.
Algunos cristales están hechos enteramente del mismo tipo de átomos «desfilando» —todos del mismo elemento—. El diamante, el oro, el cobre y el hierro son algunos ejemplos. Pero otros cristales están hechos de dos tipos distintos de átomos, también en formación de desfile y en un orden estricto: por ejemplo, alternándose. La sal (la sal común, la sal de mesa) no es un elemento, sino un compuesto de dos elementos, sodio y cloro. En un cristal de sal, los átomos de sodio y cloro desfilan juntos alternándose. De hecho, en este caso no se denominan átomos, sino «iones», pero no vamos a profundizar tanto. Cada ion de sodio tiene 6 iones de cloro alrededor, formando ángulos rectos: delante, detrás, a la izquierda, a la derecha, arriba y abajo. Y cada ion de cloro está rodeado por iones de sodio en formación idéntica a la anterior. Toda esta estructura está formada por cuadrados, y por eso si observas detenidamente un cristal de sal con una buena lupa, verás que es cúbico —la forma tridimensional de un cuadrado— o al menos tiene bordes cuadrados. Muchos otros cristales están hechos de más de un tipo de átomos «desfilando», y muchos de ellos se encuentran en las rocas, la arena y la tierra.
Sólido, líquido, gas: cómo se mueven las moléculas
Los cristales son sólidos, pero no todas las cosas son sólidas. También existen líquidos y gases. En un gas, las moléculas no están pegadas como en un cristal, sino que se mueven libremente dentro del espacio disponible, viajando en líneas rectas como bolas de billar (pero en tres dimensiones, no dos como en una mesa plana). Se mueven hasta que chocan con algo, como otra molécula o las paredes de un contenedor, en cuyo caso rebotan igual que las bolas de billar. Los gases pueden comprimirse, lo que demuestra que existe mucho espacio entre átomos y moléculas. Cuando comprimes un gas, parece «elástico» Coloca el dedo en la válvula de una bomba de bicicleta y siente cómo «aprieta» cuando la activas. Si mantienes allí el dedo, cuando lo sueltes el émbolo saldrá disparado hacia atrás. Esa elasticidad que estás sintiendo se denomina «presión». La presión es el efecto de los millones de moléculas de aire (una mezcla de nitrógeno, oxígeno y algunos otros gases) que la bomba empuja a hacia el émbolo (y hacia todas partes, pero el émbolo es la única parte que puede moverse como respuesta a ese empujón). Si la presión es mayor, el empuje también lo es. Esto ocurrirá si el mismo número de moléculas de gas se encuentran en un volumen más pequeño (por ejemplo, cuando empujas el émbolo de la bomba) También ocurre si aumentamos la temperatura, lo que hace que las moléculas de gas se muevan más deprisa.

Un líquido es similar a un gas porque las moléculas se mueven libres o «flotan» (por eso los llamamos «fluidos», mientras que los sólidos no lo son). Pero las moléculas de un líquido están mucho más juntas unas de otras que las moléculas de un gas. Si introduces un gas en un tanque sellado, ocupará hasta el último milímetro cúbico de tanque. El volumen del gas se expande rápidamente para rellenar el tanque completo. El líquido también rellena todos los huecos, pero solo hasta cierto nivel. Una cantidad fija de líquido, a diferencia de la misma cantidad de gas, mantiene un volumen fijo, y la gravedad lo empuja hacia abajo, de forma que solo rellena la parte que necesita del tanque desde abajo hacia arriba. Eso se debe a que las moléculas del líquido se mantienen cerca unas de otras. Pero a diferencia de un sólido, se deslizan por encima de las demás, por eso los líquidos se comportan como fluidos.
Un sólido no intenta rellenar el tanque; solo mantiene su forma. Eso se debe a que las moléculas de un sólido no se deslizan unas por encima de otras como las de un líquido, sino que permanecen (aproximadamente) en la misma posición con relación a sus vecinas. He dicho «aproximadamente» porque incluso en un sólido las moléculas realizan una especie de «sacudida» (más rápida cuanto mayor es la temperatura): solo que no se mueven lo suficientemente lejos de su posición en el «desfile» del cristal como para afectar a la forma del mismo.
A veces, un líquido es «viscoso», como la miel. Fluye, pero tan despacio que tarda mucho en rellenar el tanque. Algunos líquidos son tan viscosos —fluyen tan despacio— que podrían considerarse también sólidos. Las sustancias de este tipo se comportan como sólidos, aunque no estén hechas de cristales. El vidrio es un ejemplo. El vidrio debería «fluir», pero lo hace de forma tan lenta que tarda siglos en que lo notemos. Por tanto, a efectos prácticos, podemos considerar el vidrio como un sólido.

Sólido, líquido y gas son los nombres que damos a las tres fases comunes de la materia. Y muchas sustancias son capaces de pertenecer a los tres, dependiendo de la temperatura. En la Tierra, el metano es un gas (llamado a menudo «gas pantanoso», porque emana de los pantanos y a veces arde y se ilumina con una luz fantasmagórica). Pero en una luna muy lejana y muy fría del planeta Saturno, llamada Titán, existen lagos de metano líquido. Si un planeta estuviera suficientemente frío, podría tener «rocas» de metano helado. Solemos pensar en el mercurio como un líquido, pero eso solo significa que es líquido a temperaturas normales en la Tierra. El mercurio es un metal sólido si lo dejamos a la intemperie en el invierno ártico. El hierro es líquido si lo calentamos a la temperatura suficiente. De hecho, alrededor del núcleo de la Tierra hay un mar de hierro líquido mezclado con níquel líquido. Por lo que yo sé, podría haber planetas muy calientes con océanos de hierro líquido en su superficie, y quizá extrañas criaturas bañándose en ellos, aunque lo dudo. Según nuestros estándares, el punto de congelación del hierro es caliente, por eso en la superficie de la Tierra normalmente lo encontramos como «hierro frío»[1], y el punto de congelación del mercurio es frío, de manera que solemos encontrarlo como líquido. En el otro extremo de la escala de temperaturas, tanto el mercurio como el hierro se convierten en gases si los calentamos lo suficiente.
Dentro del átomo
Cuando al principio del capítulo imaginábamos cómo cortar la materia en los trozos más pequeños posibles, nos detuvimos al llegar al átomo. Un átomo de plomo es el objeto más pequeño al que aún podemos llamar plomo. Pero ¿realmente no se puede cortar un trozo de plomo? ¿Y un átomo de plomo no tendría el aspecto de un pequeño trozo de plomo? No, no tendría aspecto de un pequeño trozo de plomo. No tendría aspecto de nada. Eso se debe a que un átomo es demasiado pequeño para ser visto, incluso con un potente microscopio. Y sí, podemos cortar un átomo en trozos aún más pequeños; pero lo que obtendríamos ya no sería el mismo elemento, por motivos que veremos enseguida. Y aún más, resultaría muy difícil de hacer y requeriría una alarmante cantidad de energía. Este es el motivo por el que, a algunas personas, la frase «partir el átomo» les suena tan agorera. El primero en hacerlo fue el gran científico neozelandés Ernest Rutherford, en 1919.
Que no podamos ver un átomo y no podamos dividirlo sin convertirlo en algo diferente no significa que no podamos descubrir qué aspecto interior tiene. Tal como expliqué en el Capítulo 1, cuando los científicos no pueden ver algo directamente, proponen un «modelo» de lo que debería ser, y después prueban dicho modelo. Un modelo científico es un modo de imaginar cómo pueden ser las cosas. Por tanto un modelo del átomo es una especie de imagen mental del aspecto que debe de tener el interior de un átomo. Un modelo científico puede parecer un juego de la imaginación, pero no lo es. Los científicos no solo proponen un modelo: después lo prueban. Lo que dicen es: «Si este modelo que estoy imaginando fuera cierto, cabría esperar verlo igual en el mundo real». Predicen lo que encontraremos si hacemos un experimento concreto y tomamos medidas. Un modelo exitoso es aquel cuyas predicciones resultan ser ciertas, especialmente si sobreviven a la prueba del experimento. Y si las previsiones resultan ser ciertas, esperamos que eso signifique que el modelo probablemente representa la verdad, o al menos parte de la verdad.

A veces las previsiones no salen bien, y entonces los científicos reajustan el modelo o crean uno nuevo, y después lo prueban. En cualquier caso, este proceso de proposición y prueba de un modelo —lo que denominamos el «método científico»— tiene muchas más posibilidades de determinar cómo son realmente las cosas que los mitos más maravillosos e imaginativos inventados para explicar lo que la gente no sabía —y a menudo, tampoco podía entender—.
Un modelo anterior del átomo fue el denominado «currant bun» (panecillo de pasas), propuesto por el gran físico inglés J. J. Thompson, a finales del siglo XIX. No voy a describirlo porque fue reemplazado por el modelo más exitoso de Rutherford, propuesto por el mismo Ernest Rutherford que dividió el átomo, que vino desde Nueva Zelanda hasta Inglaterra para trabajar como alumno de Thompson, al que sucedió como catedrático de física en la Universidad de Cambridge. El modelo Rutherford, reajustado más tarde por un alumno de Rutherford, el famoso físico danés Niels Bohr, trata el átomo como un sistema solar en miniatura. Haya un núcleo en mitad del átomo que contiene la masa de su material. Y hay pequeñas partículas llamadas electrones que zumban alrededor del núcleo en «órbita» (aunque «órbita» puede no ser una palabra correcta si la comparas con un planeta que orbita alrededor del sol, porque un electrón no es algo pequeño y redondo en un lugar concreto).
Algo sorprendente del modelo Rutherford/Bohr, que probablemente refleja una verdad real, es que la distancia entre cada núcleo y el siguiente es muy grande en comparación con el tamaño de los núcleos, incluso en un trozo duro de materia sólida como un diamante. Los núcleos están muy distanciados. Este es el punto al que te prometí antes que regresaríamos.
¿Recuerdas que dije que un cristal de diamante es una molécula gigante compuesta por átomos de carbono, como soldados en un desfile tridimensional? Bueno, ahora podemos mejorar nuestro «modelo» del cristal de diamante aplicándole una escala —es decir, una idea de la proporcionalidad que mantienen en él las distancias y los tamaños—. Supón que representamos los núcleos de cada átomo de carbono del cristal no con un soldado, sino con un balón de fútbol, con electrones orbitando a su alrededor. En dicha escala, los balones más cercanos dentro del diamante estarían a más de 15 kilómetros de distancia.
Los 15 kilómetros entre los balones podrían contener a los electrones en órbita alrededor de los núcleos. Pero cada electrón, en nuestra escala «futbolística», es mucho más pequeño que un mosquito, y esos mosquitos en miniatura están a varios kilómetros de distancia del balón alrededor del que vuelan. Resulta increíble que incluso el legendariamente duro diamante esté prácticamente compuesto por
¡espacio vacío!
Lo mismo ocurre con todas las rocas, sin importar su dureza o solidez. También con el hierro y el plomo. Incluso con la madera más dura. Y es cierto en ti y en mí. Ya he dicho que la materia sólida está hecha de átomos pegados, pero en este caso «pegados» significa algo distinto, porque los propios átomos son, básicamente, espacio vacío. Los núcleos de los átomos están tan alejados que si los pusiéramos en la escala futbolística, cualquier par de ellos estaría a 15 kilómetros de distancia, con algunos mosquitos por medio.
¿Cómo es posible? Si una roca está prácticamente compuesta por espacio vacío, con la materia distanciada como balones separados por kilómetros de su balón más cercano, ¿cómo puede ser tan dura y sólida? ¿Por qué no se derrumba como un castillo de naipes cuando nos sentamos encima? ¿Por qué no podemos ver a través de ella? Si tanto una pared como yo mismo estamos hechos principalmente de espacio vacío, ¿por qué no puedo atravesarla?
De primeras suena factible. Sé que tanto la pared como mi cuerpo están hechos de átomos tan espaciados entre sí que son como balones separados por 15 km. Seguramente, sin tanto la pared como mi propio cuerpo son casi espacio vacío, debería ser capaz de atravesarla, colando mis átomos entre los de la pared. ¿Por qué no puedo?
¿Por qué las piedras y las paredes son duras, y por qué no podemos mezclar nuestros espacios con los suyos? Debemos asumir (como cualquiera que intente atravesar una pared aprenderá del modo más duro) que lo que sentimos y vemos como materia sólida es más que simplemente núcleos y electrones —«balones» y «mosquitos»—. Los científicos hablan de «fuerzas», «uniones» y «campos» que actúan de formas diferentes, tanto para mantener separados los balones como para mantener unidos los componentes de cada balón. Y son esas fuerzas y esos campos los que hacen que las cosas resulten sólidas.
Cuando hablamos de cosas realmente pequeñas como átomos y núcleos, la distinción entre materia y espacio vacío comienza a perder su significado. No es del todo correcto decir que el núcleo es «materia», como un balón, y que hay «espacio vacío» hasta el siguiente núcleo.

Definimos la materia sólida como «aquello que no podemos atravesar». No podemos atravesar una pared por esas fuerzas misteriosas que unen los núcleos con sus vecinos en una posición fija. Eso es lo que significa sólido.
Líquido significa algo similar, salvo que los misteriosos campos y fuerzas mantienen algo menos unidos los átomos, de forma que se desplazan unos sobre otros, lo que significa a su vez que sí podemos atravesar el agua, aunque no tan deprisa como podemos hacerlo con el aire. El aire, al ser un gas (una mezcla de gases, en realidad) es fácil de atravesar porque los átomos de un gas se mueven con total libertad, en vez de estar ligados unos a otros. Solo es difícil atravesar un gas si la mayoría de los átomos se mueven en la misma dirección y es la dirección opuesta la que queremos llevar nosotros. Esto es lo que ocurre cuando queremos andar en contra del viento (eso es lo que significa «viento»). Puede resultar difícil andar en dirección contraria a un vendaval, y es imposible hacerlo contra un huracán o contra el flujo artificial producido por un motor a reacción.
Imagina que estás sentado en una habitación corriente de un edificio corriente contemplando la pared. Y te da por pensar: esa pared es de hormigón y el hormigón está compuesto por átomos y los átomos son principalmente espacio vacío. Igual que tú, principalmente espacio vacío.
Seguramente podrías atravesar la pared. ¿Por qué no intentarlo? Y lo intentas.
Y entonces te estrellas contra el muro. ¿Por qué?

Es imposible atravesar la materia sólida, pero algunas partículas muy pequeñas como las que llamamos fotones sí pueden. Los rayos de luz son flujos de fotones, y pueden atravesar algunos tipos de materia sólida, los tipos que denominamos «transparentes». El modo en el que se alinean los balones en un cristal, o en el agua, o en ciertas gemas, hace que los fotones pueden atravesarlos, aunque se ralentizan un poco al hacerlo, igual que nos ocurre a nosotros cuando nos zambullimos en el agua.

Salvo algunas pocas excepciones como los cristales de cuarzo, las rocas no son transparentes, y los fotones no pueden atravesarlas. En lugar de eso, dependiendo del color de la roca, son absorbidos por esta o reflejados por su superficie, igual que ocurre con la mayor parte del resto de cosas sólidas. Algunas cosas sólidas reflejan los fotones en línea recta, y solemos denominarlas espejos. Pero la mayoría de las cosas sólidas absorben gran parte de los fotones (no son transparentes), y dispersan aquellos que reflejan (no se comportan como espejos) Nosotros las vemos simplemente como «opacas», y también percibimos en ellas un color que depende de qué tipo de fotones absorben y cuáles reflejan. En el Capítulo 7, «¿Qué es un arco iris?», retomaremos el importante asunto del color. Mientras tanto debemos ajustar nuestra visión a lo muy pequeño, y mirar dentro del propio núcleo —el balón de fútbol—.
Las cosas más pequeñas de todas
El núcleo, en realidad, no tiene forma de balón. Solo era una manera de verlo. No es redondo como un balón. Ni siquiera está claro si deberíamos hablar de que tiene algún tipo de «forma».
Quizá la propia palabra,

igual que «sólido», pierden todo su significado en cosas tan pequeñas. Y ahora estamos hablando de cosas muy muy pequeñas.
El punto final que cierra esta frase contiene cerca de un millón de millones de átomos de tinta impresa.

Cada núcleo contiene partículas más pequeñas denominadas protones y neutrones. También puedes imaginarlas como balones, si quieres, pero al igual que el núcleo, en realidad no lo son. Los protones y los neutrones tienen aproximadamente el mismo tamaño. De hecho, son muy muy pequeños, pero aun así son 1000 veces mayores que los electrones (los «mosquitos») que orbitan alrededor del núcleo. La diferencia principal entre un protón y un neutrón es que el protón tiene carga eléctrica. Los electrones también tienen carga eléctrica, contraria a la de los protones. Aquí no vamos a entrar en lo que significa exactamente «carga eléctrica». Los neutrones no tienen carga.
Como los electrones son muy muy muy pequeños (a diferencia de los protones y los neutrones, que solo son muy muy pequeños), la masa de un átomo es, a todos los efectos, la de sus protones y neutrones. ¿Qué significa «masa»? Bueno, puedes pensar en la masa como algo similar al peso, y puedes medirla utilizando las mismas unidades de medida que para el peso (gramos o libras). No obstante, el peso no es lo mismo que la masa, y tendré que explicarte la diferencia, pero lo dejaré para el próximo capítulo. De momento piensa simplemente que la «masa» es algo parecido al «peso».

La masa de un objeto depende casi por completo de cuántos protones y neutrones tengan la suma de todos sus átomos. El número de protones del núcleo de cualquier átomo de un elemento en concreto siempre es el mismo, y es igual al número de electrones que orbitan alrededor del núcleo, aunque los electrones apenas contribuyen a la masa porque son demasiado pequeños. Un átomo de hidrógeno solo tiene un protón (y un electrón). Un átomo de uranio tiene 92 protones. El de plomo, 82. El de carbono, 6. Para cualquier número posible, desde 1 hasta 100 (e incluso alguno más) existe un único elemento que tiene ese número de protones (y el mismo número de electrones). No vamos a ponerlos todos aquí, pero sería fácil hacerlo (Lalla, mi mujer, es capaz de recitarlos todos de memoria, a gran velocidad, un truco que aprendió como ejercicio de entrenamiento de la memoria y como ayuda para dormir).
El número de protones (o electrones) que posee un elemento se denomina «número atómico» de dicho elemento. De esta forma podemos identificar a un elemento no solo por su nombre, sino también por su número atómico único. Por ejemplo, el elemento número 6 es el carbono; el elemento número 82 es el plomo. Los elementos están ordenados en una tabla denominada «tabla periódica» —no voy a entrar en por qué se denomina así, aunque es interesante—. Pero ahora es momento de volver, tal como te prometí, a la pregunta de por qué cuando cortamos un trozo de plomo en trozos más y más pequeños, llega un momento en el que si volvemos a dividirlo, deja de ser plomo. Un átomo de plomo tiene 82 protones. Si lográramos dividir el átomo de forma que ya no tuviera 82 protones dejaría de ser plomo.
El número de neutrones en el núcleo de un átomo no es tan fijo como el número de protones: muchos elementos tienen distintas versiones, denominadas isótopos, con distintos números de neutrones. Por ejemplo, el carbono tiene tres isótopos, denominados carbono-12, carbono-13 y carbono-14. Los números hacen referencia a la masa del átomo, que es la suma de los protones y los neutrones. Cada uno de los tres tiene seis protones. El carbono-12 tiene seis neutrones, el carbono-13 tiene siete neutrones y el carbono-14 tiene ocho neutrones. Algunos isótopos, por ejemplo, el carbono-14, son radiactivos, lo que significa que se convierten en otros elementos pasado un tiempo concreto, a una velocidad predecible. Los científicos pueden utilizar esta característica para calcular la edad de los fósiles. El carbono-14 se utiliza para datar cosas más jóvenes que la mayoría de los fósiles, por ejemplo, antiguos barcos de madera.
Entonces, nuestra pregunta sobre cortar las cosas cada vez más pequeñas, ¿termina con estas tres partículas: electrones, protones y neutrones? No, incluso los protones y los neutrones tienen un interior. Contienen cosas aún más pequeñas llamadas quarks. Pero eso es algo de lo que no vamos a hablar en este libro. No es porque piense que no lo entenderías. ¡Es porque sé que yo mismo no lo entiendo! Estamos entrando en un maravilloso mundo de misterio. Y es importante darse cuenta de cuándo alcanzamos los límites de lo que podemos entender. No es que nunca vayamos a entender este tipo de cosas. Probablemente lo haremos, y los científicos están trabajando en ello con esperanzas de éxito. Pero debemos saber qué es lo que no entendemos y admitirlo, antes de que podamos empezar a trabajar en ello. Hay científicos que entienden al menos parte de este maravilloso mundo de lo muy pequeño, pero yo no soy uno de ellos. Yo conozco mis limitaciones.
El carbono: los andamios de la vida
Todos los elementos son especiales en distinta forma. Pero hay un elemento, el carbono, que es tan especial que quiero terminar el capítulo hablando brevemente sobre él. La química del carbono tiene incluso su propio nombre, que la separa del resto de la química: la química «orgánica». El resto de la química se denomina «inorgánica». ¿Qué tiene el carbono que lo hace tan especial?
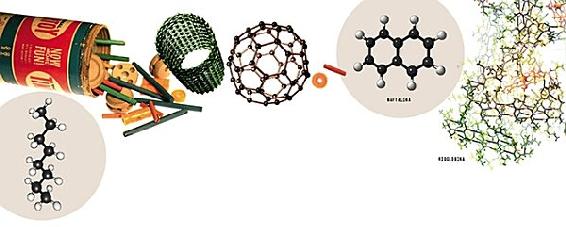
La respuesta es que los átomos de carbono se unen entre sí formando cadenas. El compuesto químico octano (en el dibujo de la izquierda), que como sabrás es un ingrediente del petróleo y la gasolina, es una cadena corta de ocho átomos de carbono (las bolas negras del dibujo) con átomos de hidrógeno (las bolas grises) sobresaliendo en los laterales. Lo asombroso del carbono es que puede hacer cadenas de cualquier longitud, algunas literalmente de cientos de átomos de carbono de longitud. A veces las cadenas forman un bucle. Por ejemplo, en el dibujo de arriba vemos la naftalina (esa sustancia utilizada para proteger la ropa de las polillas), cuyas moléculas también están hechas de carbono con hidrógeno enganchado, esta vez en dos bucles. La química del carbono es algo así como ese juego de ensamblaje llamado Tinkertoy.
En el laboratorio, los químicos han logrado crear átomos de carbono que se unen entre sí, no solo en bucles simples, sino en increíbles moléculas de tipo Tinkertoy a las que han apodado Bucky-bolas y Bucky-tubos. «Bucky» era el apodo de Buckminster Fuller, el gran arquitecto americano que inventó la cúpula geodésica. Es fácil ver la conexión si te fijas en la imagen de debajo. Las Bucky-bolas y Bucky-tubos fabricados por los científicos son moléculas artificiales. Pero muestran las formas en las que pueden unirse entre sí los átomos de carbono para crear estructuras de tipo andamio que pueden ser infinitamente grandes. (Hace poco se ha publicado que se habían detectado Bucky-bolas en el espacio exterior, en el polvo suspendido cerca de una estrella lejana). La química del carbono ofrece un número prácticamente infinito de posibles moléculas, todas con formas diferentes, y miles de ellas se encuentran en los cuerpos vivos. En el dibujo de arriba a la derecha puedes ver una molécula enorme llamada mioglobina, que se encuentra por millones en todos nuestros músculos. La ilustración no muestra los átomos individuales, simplemente los tubos que los unen.

No todos los átomos de la mioglobina son átomos de carbono, pero son estos los que se unen en esas magníficas estructuras de andamiaje. Y eso es lo que realmente hace que la vida sea posible. Si piensas que la mioglobina es tan solo un ejemplo entre miles de moléculas igual de complicadas dentro de las células vivas, no te costará imaginar que, del mismo modo que puedes construir estructuras maravillosas con el Tinkertoy, la química del carbono proporciona un gigantesco rango de posibles formas necesarias para crear algo tan complicado como un organismo vivo.
¿Aquí no hay mitos?
Este capítulo ha sido algo extraño porque no he comenzado con una lista de mitos. Esto es únicamente porque resulta dificilísimo encontrar mitos sobre este tema. A diferencia, por ejemplo, del sol, del arco iris o de los terremotos, el fascinante mundo de lo muy pequeño nunca llegó a ser noticia para los pueblos primitivos. Si te paras a pensarlo, resulta bastante natural. Ellos no tenían forma de saber que eso estaba ahí, y por supuesto no inventaron ningún mito para explicarlo. No fue hasta la llegada del microscopio, en el siglo XVI, cuando la gente descubrió que los estanques y los lagos, la arena y el polvo, incluso nuestros cuerpos, estaban repletos de criaturas diminutas, demasiado pequeñas para poder verlas, demasiado complicadas y, cada una con su forma particular, maravillosas, o tal vez aterradoras, dependiendo de cómo pienses en ellas.
Las criaturas del dibujo de esta página son ácaros del polvo —parientes lejanos de las arañas, pero demasiado pequeños para poder verlos—. Hay miles de ellos en cada hogar, arrastrándose por cada alfombra y cada cama, probablemente también en la tuya.
Si los pueblos primitivos hubieran sabido de ellos, ¡imagina los mitos y leyendas que podrían haber inventado para explicarlos! Pero antes de la invención del microscopio su existencia ni siquiera se soñaba; y por eso no hay mitos sobre ellos. Y puestos a hablar de lo pequeño, incluso un ácaro del polvo contiene más de cien billones de átomos.

Los ácaros del polvo son demasiado pequeños para que podamos verlos, pero las células de las que están hechos lo son aún más. Las numerosas bacterias que viven dentro de ellos —y dentro de nosotros— son aún menores.
Y los átomos son mucho más pequeños que las bacterias. El mundo entero está hecho de cosas increíblemente pequeñas, demasiado pequeñas para verlas a simple vista; y ninguno de los mitos o de los denominados libros sagrados que alguna gente, incluso ahora, piensa que nos fueron entregados por los dioses, las mencionan en absoluto. De hecho, cuando estudiamos esos mitos e historias, es fácil ver que no contienen ninguno de los conocimientos que la ciencia ha descubierto a base de paciencia. No nos dicen lo grande o lo antiguo que es el universo; no nos dicen cómo curar el cáncer; no explican la gravedad ni el motor de combustión interna; no nos hablan de gérmenes, ni de fusión nuclear, ni de electricidad o anestésicos. De hecho, aunque no me sorprende, las historias de los libros sagrados no contienen más información sobre el mundo que la que conocían los pueblos primitivos que comenzaron a escribirlos. Si realmente esos «libros sagrados» hubieran sido escritos, dictados o inspirados algún dios omnisciente, ¿no te parece extraño que esos dioses no dijeran nada sobre ninguna de estas cosas tan útiles e importantes?



