Ettől (novembertől) kezdve az efajta levegőnek természete felőli tudatlanságomban folytattam a kísérleteket 1775. március 1-ig. Annyira nem gyanítottam, hogy az: égetett higanyból nyert levegő egészséges, hogy nem is gondoltam a salétromos levegővel való kipróbálására; de gondolván (mint olvasóm el is képzelheti, hogy gyakran eszembe jutott ez) arra, hogy vízzel való hosszú összerázás után is a gyertya ég benne, végre eszembe jutott elvégezni a kísérletet; és egy térfogatrész salétromos levegőt adva két térfogatrésznyihez ebből a levegőből, nemcsak azt találtam, hogy csökkent a térfogata, hanem hogy éppen annyira csökkent, mint a közönséges levegő, és hogy a keverék vörössége éppen olyan volt, mint a salétromos és közönséges levegő hasonló keverékéé.
Ezek után nem volt kétségem afelől, hogy az égetett higany levegője alkalmas lélegzésre és hogy a valódi, közönséges levegőnek minden más tulajdonsága megvan benne. De nem vettem észre, amit megfigyelhettem volna, ha nem tett volna annyira elfogulttá az a fölfogás, hogy nincsen jobb levegő a közönségesnél, hogy ez a vörösség valójában mélyebb és a térfogatcsökkenés valamivel nagyobb, mint lett volna a közönséges levegőnél.
Mi több, ez az előhaladás az igazság útján visszavetett engem a tévedésbe, mert föladtam előbb kialakult föltevésemet, ugyanis hogy az égetett higany a levegőből vett magához salétromos szeszt; mert most arra következtettem, hogy ennek az anyagnak vagy a vörös ólomnak készítésénél a levegőnek minden alkatrésze egyformán, a maga arányának megfelelően szívódik belé. Mert ugyanakkor, mikor a fenti kísérletet végeztem az égetett higanyból nyert levegővel, hasonlóképpen megfigyeltem, hogy az a levegő, amelyet kivontam a vörös ólomból s kimostam belőle a fix levegőt, ugyanolyan természetű volt, a salétromos levegő éppúgy csökkentette, mint a közönséges levegőt; de ugyanakkor rejtélyesnek találtam, hogy a vörös csapadékból származó levegő hasonló módon csökkent, bár ez az anyag egészen más módon készül, mint a másik kettő. De véletlenül nem nagyon törődtem evvel a körülménnyel.
Szeretném, ha az olvasó nem unná el a »meglepetés« szó gyakori ismétlését meg más hasonló szavakét; de még egy kicsit ebben a stílusban kell folytatnom. Mert másnap még nagyobb meglepetésben volt részem, mint valaha: mivel a salétromos levegőnek és az égetett higanyból nyert levegőnek keveréke egész éjszakán át állott (mely idő alatt az egész csökkenésnek végbe kellett mennie; és következőleg, ha közönséges levegő lett volna, teljesen ártalmassá kellett volna válni, tökéletesen alkalmatlanná lélegzésre vagy égésre), úgy láttam, hogy a gyertya ég benne, sőt jobban, mint a közönséges levegőben.
Ennyi idő után nem emlékszem, mit akartam elérni evvel a kísérlettel; de azt tudom, hogy nem számítottam az igazi eredményre. Mivel elég készségre tettem szert ilyenféle kísérletek végzésében, nagyon csekély ok is rábír arra, hogy végezzem őket.
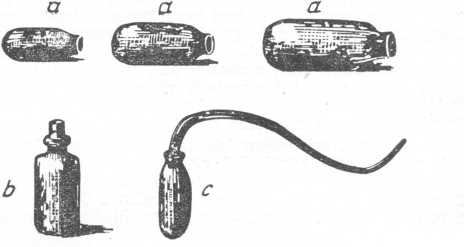
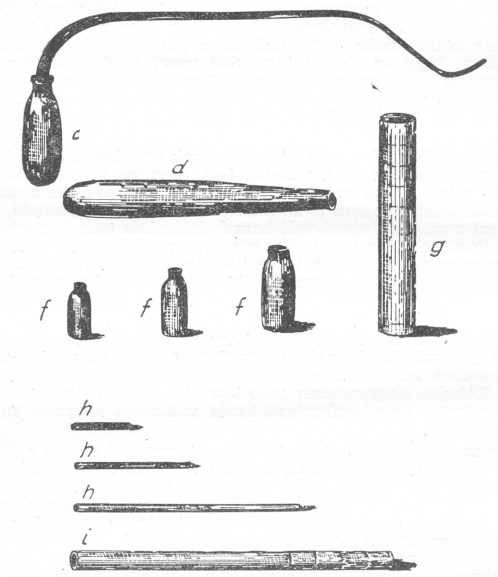
Különféle vegytani eszközök Priestley laboratóriumából. Idézett főművéből.
De ha véletlenül nem esett volna úgy, hogy más célra egy égő gyertya állott előttem, talán sohasem végeztem volna ezt a próbát; és talán elmaradt volna evvel a fajtájú levegővel végzett jövendő kísérleteimnek egész sora.
Még mindig nem lévén fogalmam ennek a jelenségnek igazi okáról, valami rendkívüli dolognak tekintettem; de olyan tulajdonságnak, amely sajátsága az ilyen anyagokból kivont levegőnek és mellékesnek tartottam; és ismerőseimnek mindig úgy beszéltem erről a levegőről, hogy lényegében azonos a közönséges levegővel.
Különösen emlékszem, amit dr. Pricenak mondtam, hogy teljes meggyőződésem szerint ez közönséges levegő, mert ennek mutatta a salétromos levegővel történt megvizsgálás; de azért mások meggyőzésére egérre volt szükségem, hogy teljessé tegyem a bizonyítékot.

Priestley készüléke szénsav előállításához. A saját magyarázó szövege: »A legalsó edénybe kell tenni a mészkövet vagy márványt, meg a vízzel hígított vitriolt, a középső edénybe az impregnálandó vizet. A pezsgés alatt a fix levegő (szénsav) a középső edénybe száll föl s ebben megmarad a víz felületén, a levegő által kiszorított víz a hajlított csövön át a legfelső edénybe emelkedik, míg a közönséges levegő eltávozik a dugóban levő csatornán át.«
E hónap 8-án egeret szereztem, s betettem egy üvegedénybe, amelyben két térfogat-uncia égetett higanyból nyert levegő volt. Ha közönséges levegő lett volna, egy ilyen teljesen felnőtt egér körülbelül negyedóráig élt volna benne. Ebben a levegőben azonban az én egerem teljes félóráig élt; és bár látszólag holtan vettem ki, úgy látszott, hogy csak nagyon megfázott; mert a tűzhöz tartottam, teljesen magához tért, és látszólag semmi baja nem történt a kísérlettől.
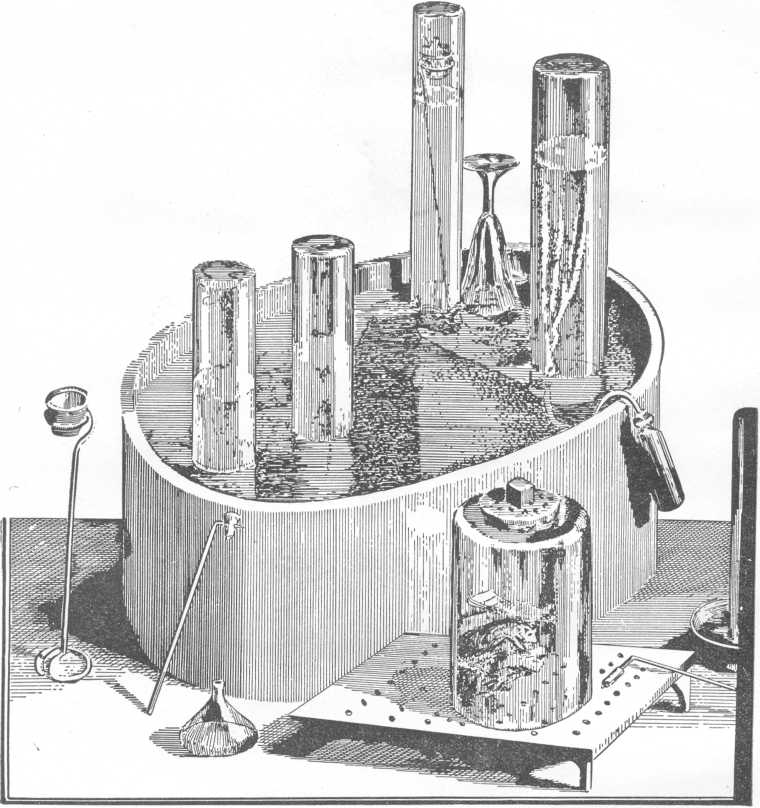
Priestley élettani kísérletei az általa fölfedezett oxigénnel; jobbról fent növényekkel; elöl lent egerekkel. Idézett főművéből.
Ez megerősítette azt a meggyőződésemet, hogy az égetett higanyból stb. kivont levegő legalábbis olyan jó, mint a közönséges levegő, de bizonyosan nem következtettem arra, hogy még jobb; mert egyik egér talán csak negyedóráig élne meg adott mennyiségű levegőben, de nem lehetetlen, hogy egy másik egér félóráig is megél benne; olyan kevéssé pontos ez a módszer a levegő jóságának megállapítására; és a magam meggyőződésére igazán nem is alkalmaztam ezt, mióta fölfedeztem azt a sokkal pontosabb és elegánsabb próbát, amivel a salétromos levegő szolgál. De ebben az esetben az volt a szándékom, hogy a legáltalánosabban kielégítő módon számolok be a kísérleteimről, amit csak megenged a dolog természete.
Ez a kísérlet az egérrel, mikor egy darabig gondolkoztam rajta, erős gyanút ébresztett bennem, hogy az a . levegő, amelybe beletettem, jobb a közönséges levegőnél; ez vett rá másnap, hogy a salétromos levegővel való próbát alkalmazzam annak a levegőnek egy kis részénél, amelyet az egér olyan sokáig lélegzett; ha ez közönséges levegő lett lett volna, meggyőződésem szerint ennek majdnem vagy egészen a lehető legmérgesebbnek kell lennie, úgyhogy a salétromos levegő nem lehet hatással rá; mikor megint csak meglepetésemre úgy találtam, hogy ámbár sokáig használódott lélegzésre, még mindig jobb volt, mint a közönséges levegő.

Priestley gázvizsgálataihoz használt készülékek. P. főművéből.
Mert mikor összekevertem salétromos levegővel a szokott kettő-egyhez arányban, 4,5 :3,5 arányban csökkent a térfogata, vagyis a salétromos levegő két kilenceddel csökkentette, mégpedig nagyon rövid idő alatt; evvel szemben sohasem tapasztaltam, hogy a leghosszabb idő alatt is akármelyik közönséges levegő többel, mint térfogatának egyötödével csökkent volna akármilyen arányú salétromos levegőtől, vagy többel, mint egynegyedével akármilyen flogisztikus folyamat hatására.
A párnámon gondolkozva ezen a rendkívüli tényen, másnap reggel még egy térfogatnyi salétromos levegőt adtam ugyanazon keverékhez, és szélső meglepetésemre úgy találtam, hogy mennyisége tovább csökkent, az eredetinek majdnem felére. Akkor egy harmadik térfogatrészt adtam hozzá, de ez nem csökkentette tovább: de egy térfogatnyival mégis kevesebb volt, mint azután is, hogy az egeret kivettem belőle.
Minthogy most már teljesen meggyőződtem, hogy ez a levegő még azután is, miután az egér félórán át lélegezte, sokkal jobb a közönséges levegőnél; és mert még mindig volt belőle másfél térfogat-unciányi, elegendő a kísérlethez, egeret tettem belé; akkor megfigyeltem, hogy az egér nem mutat semmi megrendülést attól, hogy beletettem, pedig ennek jelei láthatók lettek volna, ha a levegő nem lett volna nagyon egészséges; de nagyon jól érezte magát további félóráig, amikor nagyon erős és eleven állapotban vettem ki. Másnap megmérve a levegőt, úgy találtam, hogy 1,5 uncia-térfogatról 2/3-ra csökkent. És ezután, ha jól emlékszem (mert aznapi följegyzésemben csak annyit találok, hogy a salétromos levegő jelentékenyen csökkentette), majdnem olyan jó volt, mint a közönséges levegő. Tehát nyilvánvaló volt, hogy mivel erőteljes állapotban vettem ki belőle az egeret, a levegő nem válhatott nagyon mérgessé.
További meggyőződésül még egy egeret szereztem, s beletettem nem egészen térfogat-unciányi levegőbe, amit égetett higanyból és vörös csapadékból vontam ki (mivel ugyanolyan minőségűnek találtam a kettőt, összekevertem őket), az egér háromnegyed óráig élt benne. De mert nem voltam olyan óvatos, hogy meleg helyre tettem volna az edényt, úgy sejtem, hogy az egér a hidegtől halt meg. Minthogy azonban háromszor annyi ideig maradt életben, mint maradt volna ugyanolyan mennyiségű közönséges levegőben és én nem vártam nagy pontosságot az ilyenfajta próbától, nem találtam szükségesnek, hogy több kísérletet is végezzek egerekkel.
Mivel most már teljesen meggyőződtem az ilyenfajtájú levegő fölényes jóságáról, kezdtem megmérni tisztaságának fokát a tőlem telhető pontossággal, a salétromos levegő próbával; és elkezdtem avval, hogy egy térfogatnyi salétromos levegőhöz két térfogatnyit adtam ebből a levegőből, mintha közönséges levegőt vizsgáltam volna; és most megfigyeltem, hogy a csökkenés láthatóan nagyobb volt, mint lett volna a közönséges levegőé hasonló kezeléstől. Egy második térfogatnyi salétromos levegő eredeti mennyiségének kétharmadára csökkentette, egy harmadik térfogatrésznyi a felére. Sejtvén, hogy a csökkenés nem mehet tovább, csak még fél térfogatnyi salétromos levegőt adtam hozzá, ami még jobban csökkentette; de nem sokat, és még egy fél térfogatnyi eredeti mennyiségének több mint felét vette el; így hát ebben az esetben két térfogatnyi ilyen levegő több mint két térfogatnyi salétromos levegőt vett föl, és mégis kevesebb, mint a fele maradt meg.
Miután most már teljesen meggyőződtem ennek az újfajtájú levesének természetéről, a következő kutatásom az volt, mitől olyan tiszta, vagy filozofikusan mondva, mitől olyan deflogisztizált; és mivel a vörös ólom éppen olyan fajtájú levegőt ad, mint az égetett higany, bár közönséges levegővel van keverve és sokkal olcsóbb anyag, megvizsgáltam minden ólomkészítményt, amely hővel készült nyílt levegőn, hogy lássam, milyenféle levegőt kapok belőlük.
Ez a néhány oldalnyi mutató minden ismertetésnél jobban tájékoztatja az olvasót, főleg a vegyész-olvasót arról, hogyan állott a vegytani kutatás Priestley korában, milyen kezdetleges, tökéletlen, magakészítette eszközökkel kellett dolgoznia a kutatónak. Csodálatos, hogy mégis ilyen rendkívüli eredményeket értek el abban az időben az eszközök tökéletlensége és a kutatások eredményének helyes értelmezését akadályozó tudományos dogmák ellenére is. Viszont ne nagyon büszkélkedjünk, hogy mi már elértük a kutatási lehetőségek csúcspontját, ami a módszereket és eszközöket illeti, mert lehet, hogy a száz év múlva kutató vegyésztudós éppen úgy sajnál meg bennünket eszközeink és módszereink tökéletlensége miatt, mint mi sajnáljuk Priestleyt és kortársait.
BERGMAN
Torbern Bergman 1735-ben született Svédországnak Westgotland nevű tartományában, egy kis városban, ahol apja királyi adószedő volt. A közeli Skara városban végezte a gimnáziumot. Családja azt szerelte volna, ha pap vagy jogász lesz belőle. A fiatalember azonban inkább a matematika és a természettudomány felé vonzódott. Nagy konfliktus lehetett ez akkor közöttük. Mégis, mikor 1752-ben beiratkozott az akkor fénykorát élő upsalai egyetemre, kifelé jogot és teológiát tanult, de nagyon buzgón foglalkozott a természettudománnyal és matematikával. Előbbiekből jól akart vizsgázni, emezekből sokat akart tudni, de nemcsak kémiával, hanem fizikával, növénytannal (Linné!), rovartannal és geológiával is foglalkozott. A vége az lett a buzgóságának, hogy az egészsége nem bírta a túlzott megterhelést, egy időre abba kellett hagynia mindent. Mikor egészsége helyreállott, vége lett az alakoskodásnak, már csak kedvenc tanulmányainak élt, ebben az időben még leginkább a matematikának. 1761-ben a matematika segédtanára lett az upsalai egyetemen. Hat éven át tanított matematikát, mikor az egyetemen megürült a vegytani tanszék. Bergman mint matematikatanár is sokat foglalkozott vegytannal, most még nagyobb kedvet kapott rá, pályázott erre a tanszékre és megkapta, bár eddig egy sornyi vegytani dolgozata sem jelent meg. De ettől kezdve teljesen áttért a vegytanra, és most már semmi mással nem foglalkozott. Egymás után tette közzé beszámolóit sikeres vizsgálatokról. Európa-szerte híres vegyész lett belőle, úgyhogy Nagy Frigyes is megkörnyékezte, szerette volna megnyerni az ő porosz akadémiájának. De Bergman elhárította a megtiszteltetést, nem akart távozni a hazájából. Hazája avval hálálta meg ezt a viselkedését, hogy anyagilag bőkezűen támogatta a kutatásait. Hogy mint tanár milyen kitűnő eredményeket ért el, mi sem mutatja jobban, mint hogy tanítványai közül több neves vegyésztudós lett későbben. Azonban túl sokat dolgozott, életének utolsó tíz-tizenöt évében nagyon megrendült az egészsége, 1780-tól kezdve már súlyos beteg volt. 1784-ben halt meg, 49 éves korában, mikor egészségének javítására a wetterseei fürdőben időzött.
Bergman latinul írta meg csaknem minden munkáját s ezek a stockholmi és upsalai akadémiák évkönyveiben jelentek meg. De élete vége felé elkezdte kiadni a munkáit kötetekben »Opuscula physica et chemica« (Kisebb fizikai és vegytani munkák) címmel. Ebből három kötet jelent meg az ő életében. Ezeket németre és franciára is lefordították. Itt említjük meg mellékesen, hogy Bergman a lángész természetének megfelelően olykor átcsapott a vegytannal szomszédos területekre is, néha elég jelentékeny sikerrel. Például megvizsgálta a vulkáni kitörések alkalmával felszínre került anyagok összetételét, s így állapította meg az akkor még bizonytalan eredetű lávának vulkanikus származását. Az elsők között volt, aki kellő fontosságot tulajdonított az ásványoknál fellépő kristályalakoknak, és kereste a magyarázatát annak, miért lép föl ugyanaz az ásvány különféle kristályalakokban.
Foglalkozott az égés problémájával, s ő is. legjobb magyarázatnak találta a flogiszton-elméletet, ezért híve is maradt ennek haláláig. A flogisztont a hidrogénnel tartotta azonosnak, sőt kísérletekkel akarta megállapítani az egyes fémek flogiszton-tartalmát. De amilyen világosfejű és elfogulatlan tudós volt, kétségtelenül hűtlenné vált volna kedvenc elméletéhez, ha élete utolsó tíz évének egészségi állapota meg nem akadályozza abban, hogy behatóbban foglalkozzék azokkal az új megismerésekkel, amelyek megdöntötték a flogiszton-elméletet.
Mint ennek a kornak majdnem minden vegyészkutatója, Bergman is sokat foglalkozott a gázokkal. Elsősorban a szénsav vegyi tulajdonságait kutatta, amelyet ő levegősavnak nevezett. Ügy állította elő, hogy mészpátot oldott híg kénvasban. Valódi savnak mondotta, mert a kék lakmuszt megvörösítette és alkáliákkal sókat adott. Elég pontosan meghatározta a fajsúlyát, és rájött arra is, hogy állandóan megtalálható a levegőben, ezért is nevezte levegősavnak. Ilyen kutatásai közben Bergman néhány jó módszert dolgozott ki, amelyeknek hasznát vették későbbi vegyészek is.
Nagy érdemei vannak Bergmannak az ásványvizek kutatása körül, nem azért, mintha pontosabban mutatta volna ki ezek alkatrészeit, hanem mert újabb módszereket alkalmazott a vizsgálatainál. Nagyon fontosaknak tartotta az ásványvizek légnemű alkatrészeit, s utasításokat adott, hogyan kell fölfogni és megvizsgálni ezeket, hogyan lehet elkülöníteni a légköri levegőt a szénsavtól és kénhidrogéntől. A gáz alakú alkatrészek után következnek a szilárd alkatrészek, ezeket oldja alkoholban, hideg és forró vízben; minőségi és mennyiségi meghatározásukra azokat az újabb analitikai módszereit alkalmazza, amelyekről alább lesz szó. Vizsgálta a tenger sótartalmát is, s ennél főleg az érdekelte, hogy egyforma-e ez a sótartalom a különböző mélységekben. A konyhasón kívül a magnéziumkloridot és a mészszulfátot is megtalálta a tengervízben oldott sók között.
Minthogy Svédország már akkoriban is jelentékeny vastermelő ország volt, Bergman foglalkozott az ismert vasfajták vegyi vizsgálatával is. A kovácsolt vas, öntöttvas és acél közötti eltérések vegyi okait kutatta, az általa bevezetett analitikai eljárást alkalmazva ezeknél a vizsgálatoknál is. Először hígított kénsavban oldotta a vasfajtákat, s megfigyelte, melyiknek oldásánál mennyi hidrogéngáz fejlődik. Úgy találta, hogy a kovácsolt vas fejleszti a legtöbb, az öntöttvas a legkevesebb hidrogént, az acél közepes mennyiségűt. Ebből arra következtetett, hogy a kovácsolt vas a legtisztább, az öntött a legkevésbé tiszta vas. Evvel egyezően kovácsolt vas adja a legkevesebb, öntöttvas a legtöbb maradékot az oldásnál. Megvizsgálta a maradékot, s megállapította, hogy ez grafit, illetve szén, tehát a vas tulajdonságai a széntartalomtól függenek. Némi módosítással ugyanezt tartja a mai metallurgia is. Bergman állapította meg azt is, hogy bizonyos vasfajták azért törékenyek, mert foszfor van bennük, s a foszfor eltávolítására már ő ajánlotta a mész-adalékot. A ma oly nagy arányokban alkalmazott Thomas-eljárás szintén mészszel dolgozik.
Láttuk, hogy Boyle már a XVII. században bevezette a nedves úton történő elemzést. Bergman alaposan kidolgozta az elemzésnek ezt a módszerét, s evvel hatalmas lökést adott a vegytan haladásának. Még a mai vegyész is a Bergman által lefektetett alapokon végzi az elemzéseket. Új vizsgálószereket (reagenseket) keresett, gondosan megvizsgálta ezeknek tulajdonságait, alkalmasságát, s táblázatokba foglalta össze a reakciókat, a csapadékok minőségét és színét, oldhatóságát stb. De jellemző volt az ő módszerére, hogy nem is akarta izoláltan megkapni a vegyületek alkatrészeit, csak minden alkatrészt át akart vinni más vegyületbe, amelynek összetétele jól ismert, hogy aztán így következtessen. Ha valamely anyag nem oldódott vízben, akkor porrátörve sósavval, kénsavval, salétromsavval kezelte. Sok anyaggal így sem boldogult, ilyen esetekhez föltalálta a feltárás módszerét, ami nála még abban állott, hogy hamuzsírral olvasztotta össze az illető anyagot. Ilyen nehezen hozzáférhető anyagok voltak például a kovasavas vegyületek (szilikátok). Bergman jellemző reagensei voltak: szénsav kimutatásához mészvíz, kénsav kimutatásához báriumklorid.
Bergman mennyiségi elemzéseket is végzett, bár sokszor érthetetlenül nagy tévedésekkel. Így sok kristályvizet talált olyan ásványokban, amelyekben egyáltalán nincs is víz, például a mészpátban 11%-ot, a witheritben 28%-ot! Evvel szemben néhány mennyiségi elemzése meglepően pontos, ha figyelembe vesszük, hogy akkor még nem voltak analitikai mérlegek, amelyekkel a milligramm töredékét is mérni lehet. Így például a gipsz és kristályos szóda összetételét a következőnek találta (zárjelben a mai érték):
|
Szóda |
Gipsz |
||
|
Fém |
........... 20% (21,8) |
Fém |
........... 32% (32,9) |
|
Sav |
.......... 16% (15,4) |
Sav |
.......... 46% (46,3) |
|
Víz ____ |
......... 64% (62,8) |
Víz ____ |
.......... 22% (20,8) |
|
100% 100 |
100% 100 |
Sok ásványon is végzett mennyiségi elemzést, de eredményei csaknem valamennyinél nagyon rosszak. De hát nagyon nehéz is az ásványok elemzése és Bergman elsőnek foglalkozott evvel a dologgal.
Külön reagenseket keresett ki az ásványvizek elemzéséhez (De analysi aquarum, 1778). Rájött, hogy a vérlúgsó kék csapadékot ad a vassal, barnát a rézzel és fehéret a mangánnal. A mész reagense volt az oxálsav, a klóré az ezüstoldat stb. A különféle sókat alkohollal igyekezett elkülöníteni, az ásványvizek alkatrészeit lehetőleg oldhatatlan vegyületekbe próbálta átvinni.
Bergmannak eddig fölsorolt újításai is igen nagy jelentőségűek voltak a vegytan reformja szempontjából, de kortársai szemében mégis a vegyrokonságra vonatkozó új vizsgálatai tették híres vegyésszé. Evvel a kérdéssel Geoffroy foglalkozott elsőnek behatóbban (1. ott), s már ő kidolgozott vegyrokonsági táblázatokat, amelyeket a további tapasztalatok alapján módosítottak. De ezeknek a táblázatoknak az volt a bajuk, hogy csak közepes hőmérsékletekre voltak megállapítva, főleg a savakra és lúgokra vonatkozóan, míg például a kén rokonságát a fémekhez magas hőfokokon állapították meg. Ez nagyon bizonytalan helyzetet teremtett. Bergman revízió alá vette az egész kérdést. Először is tisztázni akarta, milyen fizikai erő hozza létre a vegyrokonságot. Akkoriban még friss volt Newton nagyhatású gravitációs elmélete s nyilván ennek hatása alatt mondotta Bergman, hogy a vegyrokonság tulajdonképpen a legkisebb részecskék egymáshoz való vonzódásán alapul. Különféle anyagok kisebb vagy nagyobb vonzódást mutatnak egy bizonyos anyag iránt. Ő így fejezi ki ezt: "Ha egy AB vegyületre egy harmadik C anyag van hatással, amely B-t kiszorítja a vegyületből és helyette maga lép vegyületbe A-val, akkor az AB helyett az AC új vegyületet kapjuk". Ez nem egyéb, mint a mai értelmű cserebomlás kifejezése és indokolása. Tehát minden anyagnál csak azt kell megvizsgálni, kiszorít-e más anyagokat a vegyületeikből.
Bergman számtalan elmésen kigondolt és alapos kísérletet végzett az egyes anyagok vegyrokonságának megállapítására. így jutott el ahhoz, hogy nem kevesebb, mint 59 anyagra dolgozta ki a vegyrokonsági táblázatot, íme a káliumra vonatkozó táblázata:
|
oldatban: |
Kálium |
összeolvasztásná l: |
|
kénsav |
foszforsav |
|
|
salétromsav |
bórsav |
|
|
sósav |
arzénsav |
|
|
foszforsav |
kénsav |
|
|
arzénsav |
salétromsav |
|
|
ecetsav |
sósav |
|
|
bórsav |
ecetsav |
|
|
kénessav szénsav |
Ez a táblázat így értelmezendő: Oldatban, vagyis közönséges hőmérsékletnél a kálium a kénsavval van legerősebb vegyrokonságban; más szóval, ha bármilyen savas káliumvegyülethez kénsavat adunk, ez kiszorítja a másik savat, és maga lép vegyületbe a káliummal. De magas hőmérsékleten a kálium a foszforsavhoz vonzódik legjobban. Bergman fölfogása szerint tehát a vegyrokonság a hőmérséklet függvénye. Megpróbálta számokkal is kifejezni a vegyrokonsági értékeket, de ilyen irányú kísérletezése sikertelen maradt. A kor minden vegyésze elfogadta Bergmannak ezt a fölfogását a vegyrokonságra vonatkozóan, s ez a nézet maradt uralkodó a XIX. század elejéig, amikor a határozott vegyi arányok törvénye lett uralkodóvá. De maga a vegyrokonság fogalma ma is él, csak más tudományos értelmezést és alapot kapott.
SCHEELE
A másik, még nagyobb svéd vegyész, egyszersmind a flogiszton-korszak utolsó alakja Scheele. Vele befejeződik ez a vajúdási korszak, hogy vége legyen a hajnalodásnak s megjöjjön az igazi világosság. Talán még jobban előkészítették volna — már mint Bergman és Scheele — ezt az új korszakot, ha sajnálatos párhuzamosság nincsen az életükben, azzal, hogy mindkettő túl korán halt el. Bergman csak 1768-ban kezdett tulajdonképpen vegytannal foglalkozni, harminchárom éves korában, s negyvenkilencedik évében már meghalt; láttuk, mennyire vitte e másfél évtized alatt. Scheele pedig csak negyvenhárom évig élt, örök kárára a tudománynak.
Carl Wilhelm Scheele Stralsundban, a kis porosz városban született 1742-ben mint hetedik gyerek. Apja kereskedő volt. Itt járta az elemi- és középiskolát, nem árulva el semmi különösebb tehetséget. Apja tanárnak vagy papnak akarta adni, de a fiúnak nem volt kedve ehhez, ellenben rajongott a gyógyszerész-mestenségért. Végre is az ő akarata érvényesült, tizenöt éves korában beállott tanoncnak egy gothenburgi patikába. Nemcsak a tanoncéveit töltötte el itt, hanem még azután is ott maradt néhány évig. Nem közönséges tucatpatikus lett belőle, hanem magánszorgalomból elsajátította kora egész vegytani tudását. Amit csekélyke fizetéséből meg tudott takar!tani, azt arra költötte, hogy megvásárolta Stahl, Neumann, Kunkel, Lemery és más nagy vegyészek könyveit. Nemcsak megtanulta alaposan, ami ezekből a könyvekből elsajátítható volt, hanem minden szabad órájában kísérletezett is. Nagy ügyességre tett szert, főleg eszközök és készülékek házi összeállításában. Nehezen haladt előre. 1765-ben elment Gothenburgból, de még hét évig volt patikussegéd néhány nagyobb városban, főleg Malmöben és Stockholmban.
Már-már úgy látszott, hogy szokatlan tudása ellenére sem fogja sokra vinni. Végre 1773-ban — még mindig gyógyszerészsegédi minőségben — Upsalába került, a híres egyetemi városba. Itt megismerkedett Bergmannal is, de egyelőre ennek sem vette hasznát. Valami különös véletlen hívta föl a szakkörök figyelmét arra, hogy Scheele nem olyan közönséges gyógyszerész, aki tucatmértékkel mérhető. Akkoriban nem gyárak látták el szerekkel a patikákat, hanem a gyógyszerészek csaknem mindent maguk készítették. Scheele főnöke egyszer valami ilyen laboratóriumi munkát végzett; hosszabb időn át salétromot tartott olvadt állapotban mérsékelt melegen; észrevette, hogy ez az olvadt salétrom kihűlés után semleges maradt s ecetsavval kezelve vörös párákat bocsátott ki. A gyógyszerész nem tudott magyarázatot erre. Szólt róla egy Gahn nevű fiatal vegyésznek, aki későbben híres ember tett, de ő sem értette a dolgot. Gahnt ingerelte a kérdés, megemlítette a nagy Bergmannak, de ez sem tudott magyarázattal szolgálni. Végre is Scheele patikussegéd úr magyarázta meg, miféle jelenség ez: van a salétromsavnak egy rokona, a salétromos sav, a kálium evvel is sót alkot, de ebben a vegyületben a bázis és sav nem nagy vegyrokonságban vannak egymással, ecet hatására a sav elválik a lúgtól s mint vörös pára eltávozik.
Amint Gahn meghallotta ezt a magyarázatot, nagyon kézzelfoghatónak találta s mindjárt tudomására hozta Bergmannak. Ez rögtön látta, hogy annak a patikussegédnek szokatlanul széleskörű vegyi ismeretei lehetnek, ha tud olyasmiről is, amiről maga sem hallott. Gahnnal megüzente Scheelenek, hogy szeretne közelebbről megismerkedni vele. Minden más fiatal vegyész oda lett volna a boldogságtól, de Scheele elutasította a meghívást. Volt is rá látszólag egy kis oka. Még mikor Stockholmban segédeskedett, dolgozatot írt a borkősavról és vegyületeiről, kísérleteit ismertette benne. Bergmannak küldte be a dolgozatot avval a kéréssel, hogy terjessze a stockholmi akadémia elé. Scheele sokáig nem hallott a dolgozata sorsáról, azt hitte, hogy Bergman nem méltatja semmire. A másolatát elküldte Retzius akadémiai adjunktusnak, s ez nyomdafestéket is kapott az akadémia kiadványai között — de nem úgy, ahogyan Scheele várta. Retzius átírta a dolgozatot olyan módon, mintha nagyrészt ő végezte volna ezeket a vizsgálatokat. Scheele úgy érezte, hogy csöbörből vederbe esett, a nagyfejűek mindenképpen elgáncsolják. Ezért neheztelt Bergmanra, s csak akkor ment el hozzá végre, mikor ez azt üzente neki, hogy tisztán feledékenységből tette félre a dolgozatát. Akkor hamarosan nagyon megbarátkoztak, és Scheele ennek köszönhette, hogy végre érvényesült, mert Bergman igazán tőle telhetően támogatta minden vizsgálódását.
Scheele 1775-ben elment Köpingbe, mert Upsalában nem volt megélhetése. Köpingben átvette egy gyógyszertár vezetését, majd ennek tulajdonosa lett 1777-ben. Ez a gyógyszertár csak olyan szerény megélhetést biztosított neki, hogy nem futotta volna a tudományos kísérletek költségeire is, ha a stockholmi akadémiától nem kap egy kis évi támogatást. Ez azonban elég kicsi összeg volt, s így bámulnunk kell Scheele lángelméjét és kitartását, hogy mégis eljutott az alább ismertetendő nagy fölfedezésekhez. Már külföldön is jó híre volt — sőt jobban ismerték mint otthon —, mikor 1786-ban váratlanul, fiatal korában elhunyt.
Ami az írásait illeti, meglehetősen gondatlan ember volt, nem igen törődött avval, hogy az ő nevéhez fűződjék az, amit ő fedezett föl. így már az életrajzában láttuk, hogy a borkősavval végzett vizsgálatait Retzius tulajdonította el; de megtette ezt vele Bergman is, aki a sóskasavra vonatkozó Scheele-vizsgálatokat közölte a szerző nevének megemlítése nélkül. Scheele érdeme volt a foszfor fölfedezése a csontokban, ez meg Gahn nevéhez fűződik. Írásai többnyire a stockholmi akadémia évkönyveiben jelentek meg. 1777-ben önállóan jelent meg németül egy kisebb könyve: »Chemische Abhandlung von der Luft und dem Feuer« (Kémiai tanulmány a levegőről és a tűzről). Sok munkája jelent meg angol és francia fordításban is. A »Luft und Feuer« a főműve. Az erre a munkájára tartozó kísérleteket 1768 és 1773 között végezte. A kéziratot már 1775 végén átadta Swederus könyvkereskedőnek kinyomtatás végett, de Scheele nagy bosszúságára csak 1777-ben jelent meg. Ebben írja le, hogyan fedezte föl az oxigént. Kétségtelen, hogy ebben megelőzte Priestleyt, mert Scheele már 1773-ban tisztán előállította és megvizsgálta az oxigént, míg Priestley csak 1774 augusztusában kezdte meg kísérleteit higanyoxiddal. De Priestley előbb hozta nyilvánosságra az eredményeit. (Itt említjük meg, hogy ámbár a svédek mindig honfitársuknak tartották Scheelét, kétségtelenül német volt az anyanyelve. Nördenskjöld 1892-ben kiádta a levelezését és laboratóriumi följegyzéseit, ezek túlnyomó része német nyelvű. A »Feuer und Luft« is német nyelven jelent meg először Upsalában).
Wilhelm Ostwald, az újkor nagy német vegyésze, azt mondja az általa újból kiadott »Feuer und Luft«-hoz írt jegyzeteiben, hogy Scheele egyike a valaha élt legtehetségesebb vegyészeknek. A vegytan története alig tud fölmutatni másik vegyészt, akiben ilyen mértékben lett volna meg a különleges képesség, hogy minden folyamatban meglássa a jellemzőt, megoldja a tulajdonságaikban addig ismeretlen anyagok problémáját. Vegytani célkitűzése is tökéletes. A »Feuer und Luft« legelső mondata így hangzik: "A testeket ügyesen alkatrészeikre bontani, ezek tulajdonságait fölfedezni és különböző módon összetenni őket, ez a tárgya és főcélja az egész vegytannak".
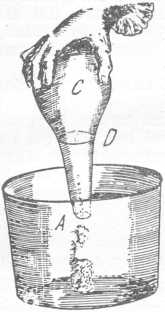
Scheele levegőelemzési eljárása
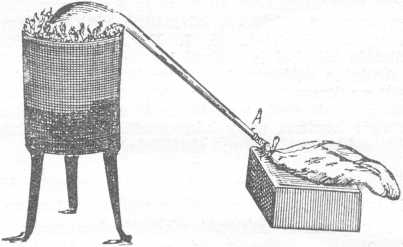
Scheele oxigénelőállítási módszere
Scheelének a levegővel végzett egész kísérletező munkája annak bizonyítására irányult, hogy a levegő nem egységes test, hanem két különböző gázból áll. Eljárása eltért Priestleyétől, mert ő bizonyos mennyiségű levegőt olyan anyaggal kezelt, amely elnyelte az egyik alkatrészt, s akkor a másik alkatrész mindig ugyanolyan mennyiségben és tulajdonságokat mutatva maradt vissza. Priestley többnyire vörös higanyoxidból, Scheele barnakőiből (mangánszuperoxidból) állította elő az oxigént, illetve a »tűzlevegőt«,. ahogyan ő nevezte. Mint tettük Priestleynél, vegyük át tőle is szó szerint a döntő kísérleteket:
»Első kísérlet 32. §. Annyi tömény vitriololajat kevertem finoman szétdörzsölt barnakőhöz, hogy sűrű pép lett belőle. Ezt a keveréket nyílt tűzön űztem ki egy kis retortából. Felfogó helyett légüres hólyagot használtam, és hogy a felszálló párák meg ne támadják a hólyagot, egy kevés mésztejet öntöttem belé. Amint a retorta feneke izzani kezdett, levegő ment át, amely lassanként megtöltötte a hólyagot. Ez a levegő mutatta a tiszta tűzlevegőnek minden tulajdonságát.
Második kísérlet. 33. §. Mikor két rész finoman pofrátört barnakövet desztilláltam egy rész foszforos húgysavval (Scheele így nevezi a foszforsavat) az előbbi §-ban jelzett módon, szintén tűzlevegőt kaptam.
Harmadik kísérlet. 34. §.
a) Az orvostanban használatos fehér magnéziát oldottam föl választóvízben; ezt az oldatot beszáradásig elpárologtattam. Erre desztillálás céljából kis retortába tettem ezt a sót, amint a 32. §-ban elmondtam. Még mielőtt a retorta izzani kezdett, a salétromsav elvált a magnéziától, mégpedig vérvörös párákban, és ugyanabban a pillanatban a hólyag duzzadni kezdett.. Az így kapott levegő az én tűzlevegőm volt.
Így látni naponta, hogy a salétromsav vérvörösen elpárolog, ha a hő segítségéivel elválik azoktól a fémektől, amelyek oldva voltak benne.
b) Előbbi módon desztilláltam a higanyos salétromot (mai neve: higanynitrát), amíg a salétromsav elvált a visszamaradt vörös csapadéktól. Itt is a mi tűzlevegőnket kaptam. A salétrom már képes arra, hogy felbontsa a meleget. Honnan ered a forrása a tégelyben folyó és sötéten izzó salétromnak? Nem látni, hogy füst vagy pára szállana föl belőle, és a nyílt tégely fölött repkedő szénpor mégis meggyullad és ragyogóan ég? Honnan van, hogy egy vas retortában félórán át izzó folyásban megtartott ilyen salétrom kihűlés után a szabad levegőn megnedvesedik és szétfolyik, és mégsem mutatja nyomát lúgos sónak? Mi az oka annak, hogy ez a folyósított salétrom, növényi savakkal keverve vagy dörzsölve, olyan hamar elereszti illó savát? Miután megismertem a hő belső alkatrészeit, nem esik nehezemre válaszolni erre. Ha a vegyészek a múlt században pontosabb vizsgálatra méltatták volna a levegőhöz hasonló buborékos folyadékokat, amelyek olyan sok műveletnél mutatkoznak, hol állanánk már? Ők mindent testileg akartak látni és cseppeket összegyűjteni a felfogóban. Csak most jutottak jobb belátásra és kezdték vizsgálni a levegőt világosan; és ki nem látja be a hasznot, amivel az ilyen kísérletek járnak?
Azt mondtam, hogy már maga a salétrom fölbontja a hő anyagát. (Scheele finom anyagnak vélte a hőt.) A következő kísérlet bizonyítja ezt.
Negyedik kísérlet. 35. §. Egy uncia tisztított salétromot tettem üvegretortába desztillálás céljából és fölfogó helyett megnedvesített, légüressé tett hólyagot használtam. Amint a salétrom izzani kezdett, forrásba is jutott, s ugyanakkor a hólyag felduzzadt az átmenő levegőtől; addig folytattam a desztiliálást, amíg a forrás megszűnt a retortában és amíg a salétrom át akart hatolni a puha retortán. A hólyagban tiszta tűzlevegőt kaptam, mely húsz unciányi víz térfogatát foglalta el. Ez a legolcsóbb és legjobb módszer tűzlevegő előállítására."
Scheele ezekkel a kísérletekkel fedezte föl az oxigént. Sok olyan kísérletet is végzett, amelyekkel megállapította az oxigén mennyiségét a levegőben. Így például kénmáj oldatát (hamuzsírral összeolvasztott kén) üres palackba tette, ezt megfordította, és szájával lefelé vízzel telt kis edénybe állította. Két héten át hagyta a palackot ebben a helyzetben. A kénmájnak az a tulajdonsága vám, hogy mohón magába szívja az oxigént. Két hét múlva Scheele víz alatt kivette a dugót a palackból, a víz rögtön belenyomult, így derült ki, hogy húsz rész levegőben négy rész tűzlevegő van, tehát 1/5 résznek. Körülbelül hasonló eredményt kapott, foszfor, vasreszelék stb. alkalmazásával. Akkor is 1/5-nek találta a térfogatcsökkenést, ha hidrogént égetett el zárt levegőben.
Mikor először állította elő az oxigént barnakőből, üveget töltött meg evvel a gázzal, s meggyújtott kis gyertyát tartott belé. "Alighogy ez megtörtént,a gyertya kezdett nagy lánggal égni és olyan fényesen, hogy a szem káprázott tőle." De ez csak egy darabig tartott, a gyertya azután elaludt, mert az égést tápláló »tűzlevegő« elfogyott. Ha az így visszamaradt gázhoz újból tűzlevegőt kevert, ez a keverék mindenben hasonlított a közönséges légköri levegőhöz. Azt a levegőt, amely már alkalmatlanná vált az égésre, "romlott levegőnek" nevezte. Csak későbben különböztették meg ezt mint nitrogént. Így következtetett Scheele arra, hogy a légköri levegőnek egyik alkatrésze az, amely táplálja a tüzet. »Ez olyan levegőfajtával van keverve a légköri levegőben, amelyik semmi vonzódást nem mutat az éghetőhöz; ez a rész az, amely meggátolja a túl gyors és heves égést.«
Mint Priestley, úgy Scheele sem elégedett még az oxigén fizikai és vegyi tulajdonságainak kiderítésével. Fölismerte óriási szerepét az élő világban is. Kísérletileg megállapította, hogy az állatok tűzlevegőt használnak el és levegősavat (szénsavat, C02) termelnek. Könyvének 85. paragrafusában olvassuk a legszebb élettani kísérletét:
»Egy húsz unciányi vizet befogadó üvegbe, közel a fenekéhez, letört reszelő hegyével lyukat fúrtam (35. ábra, A). Ebbe az üvegbe tettem egy kis darab oltatlan meszet s dugóval zártam el a nyílását, amelyen előbb B csövet dugtam át; ezt a dugót szurokgyűrűvel vettem körül s a C cukorüveget tettem föléje megfordítva, ebbe pedig előzőleg egy nagy méhet tettem és számára egy kis mézet papírra kenve; de hogy levegő ne hatolhasson be a szurokgyűrű között, jól rányomtam a cukorüveget; utóbb az üveget a D tálba tettem, ebbe annyi vizet öntöttem, hogy félig elfödte az üveget; mikor láttam, hogy a víz fölemeli az üveget, egy kis súlyt helyeztem a cukorüvegre. A kis A nyíláson át a víz mindennap fölszállott egy kicsit az üvegbe; olykor mozgattam is egy kicsit az üveget, hogy a mésztej fölött képződött bőr megrepedjen. Hét nap elteltével a víz E-ig emelkedett, a méh pedig meghalt. Néha két méhet is tettem a C üvegbe, amikor ugyanannyi levegő felényi idő alatt alakult át levegősavvá.
Hernyók és lepkék ugyanúgy viselkedtek.-"
Scheele kísérlete a méhvel.
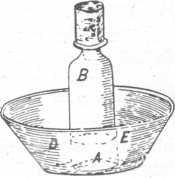
A mai életbúvár sem igein tud jóval elmésebb kísérletet kiagyalni annak bizonyítására, hogy az állatok oxigént fogyasztanak és szénsavat termelnek. Ám Scheele kísérletezett növényekkel is, ahol a megfordított folyamatot találta. Íme könyvének 86. §-a:
"Egy kis lombikba, amely huszonnégy uncia vizet volt képes befogadni, sok borsót tettem, s annyi vizet öntöttem rá, hogy ez félig elfödte a magvakat; erre elzártam a lombikot. A borsómagok kezdtek gyökeret ereszteni, és felnőttek. Mikor tizennégy nap múlva úgy láttam, hogy már nem nőnek tovább, víz alatt, szájjal lefelé, kinyitottam a lombikot, és úgy találtam, hogy a levegő se nem csökkent, se nem gyarapodott. De a mésztej elnyelte a negyedrészét, a megmaradt levegő pedig eloltotta a gyertyát. Friss gyökereket, gyümölcsöket, füveket, virágokat és leveleket, mindegyiket külön, tartottam lombikokban, s néhány nap múlva mindig azt láttam, hogy a levegő negyedrésze levegősavvá alakult át. Ha legyeket teszünk ilyen levegőbe, rögtön meghalnak."
De végzett Scheele a mai értelemben vett biokémiai kísérleteket is annak kiderítésére, hogy mi köze van a vérnek az oxigénhez. A 89. §-ban írja le ezt a kísérletét:
"A borsómagvak által elrontott levegőt tűzlevegővel kevertem és egy hólyagot töltöttem meg vele. Mikor erre tisztán kifújtam a tüdőmben levő levegőt, annyiszor beszívtam ezt az újból összetett levegőt, ahányszor lehetett. Úgy találtam, hogy nagyon kevés levegősav volt benne, és amint ez elvált tőle, eloltotta a tüzet. Azt hiszem, a tüdőerekben levő levegőnek kell tulajdonítani azt a hatást, amellyel a tüdős állatok vannak a levegőre. A következő kísérlet indít erre:
Ismeretes, hogy a frissen kieresztett vér, ha szabad levegőn áll, a felületén szép; vörös színt kap és hogy az alsó részek szintén megvörösödnek, ha levegő éri őket. Talán a levegő okoz itt változást? Egy lombikot harmadrészéig megtöltöttem frissen, kieresztett ökörvérrel, gondosan összekötöttem egy hólyaggal, és többször fölráztam a vért. Nyolc órával későbben nem találtam levegősavat ebben a levegőben, a térfogata sem csökkent, de a gyertya lángja rögtön kialudt benne. Télen végeztem ezt a kísérletet, amiből ki lehet venni, hogy nem rothadásnak tulajdonítható ez a hatás, mert azonfelül is frissnek találtam ezt a vért még további hat nap múlva is, márpedig minden rothadás levegősavat termel."
Így terelődött Scheele figyelme a szerves anyagok, főleg a szerves savak kutatására. Előtte alig foglalkoztak ezekkel a vegyületekkel, mert az akkori kutatási módszerek mellett ez még nagyon nehéz dolog volt. Például azt a kevés szerves savat is, amit ismertek, csak szublimálással tudták elkülöníteni. Scheele lángesze kellett egy jobb módszer fölfedezéséhez. Ő krétával csapta ki a savakat a növényi nedvekből, ami többnyire oldhatatlan vegyületet adott, tehát kivált a vízből. Az új vegyületet sósavval, ha nehezen oldható volt, akkor kénsavval bontotta föl. De más kötőanyagot is alkalmazott, például ólomoxidot.
Így fedezte föl a borkősavat, sóskasavat, almasavat, citromsavat, gallussavat stb.; sőt a sóskasavat mesterségesen is előállította cukorból salétromsavval. Nagy sikerrel kutatta az állati savakat is, ő fedezte föl a húgysavat és tejsavat, pedig ezek nagyon gyakori anyagok az állatvilág termékeiben. Húgykővizsgálatok vezették rá a húgysavra. A tejsavat már régebben ismerték, de Scheele vizsgálta meg először pontosan. 1782-ben egyszer vérlúgsót bontott fel kénsavval, akkor fedezte föl a kéksavat (ciánhidrogént). Erről mintaszerű értekezést írt. Vizsgálta a zsírok viselkedését lúgokkal szemben, és sikerült neki olívaolajból glicerint kiválasztani, amit ő »olajcukornak« nevezett.
A fentiek után Scheelét kell tartanunk a szerves vegytan megalapítójának, és igazat kell adnunk Ostwaldnak, aki azt mondja róla, hogy előtte egyetlen vegyész sem akadt, aki annyi új ismerettel gazdagította volna a vegytant. És mindezt negyvenhárom éves koráig, .amikor a halál könyörtelenül véget vetett ennek a rendkívül termékeny életnek.
Minthogy kutatásainak fő problémája az égés mibenléte volt, Scheele szép eredményekhez jutott el a fizika s a fizikával határos vegytan területén is. Így a legelső természetbúvárok közé tartozott, akik különbséget tettek testhő és sugárzóhő között. Kimutatta, hogy a sugárzóhő egyenes vonalban távozik a hőforrástól, és csiszolt fémlapról ugyanolyan törvények szerint verődik vissza, mint a fény, vagyis a beesési szög egyenlő a visszaverődési szöggel. A sugárzóhő abban is megegyezik a fénnyel, hogy légáramlatok nem térítik el az útjából.
Ugyancsak az elsők között volt a fény vegyi hatásainak tanulmányozásában. Schulze német orvostanár már 1727-ben észlelte, hogy az ezüsttartalmú csapadékok érzékenyek a fény iránt. Scheele klórezüsttel kísérletezett, s úgy találta, hogy ez a napfény hatására megfeketedik, vagyis redukálódik. Evvel a megállapításával rakta le a fényképezés alapjait, bár ennek fölfedezése még félszázadig váratott magára. Ő ugyanazt jelentette a fényképezésnek, mint Hertz a rádiónak. Ő fedezte föl azt is, hogy a fehér fény különféle színű sugarai nem egyforma hatással vannak az ezüstsókra. Félreérthetetlenül megállapítja: "Tegyünk üvegprizmát az ablak elé, s engedjük a földre esni a megtört fényt. Ebbe a színes fénybe tegyünk egy darab papírt, amelyet klórezüsttel vontunk be. Ez a vegyület az ibolyaszínben sokkal előbb feketedik meg, mint a többiben."
És itt jutunk el Scheele különös flogiszton-értelmezéséhez, mert mindvégig ragaszkodik ehhez az elmélethez. Mint fürkésző elme, természetesen keresi, honnan ered a fény redukáló hatása. Nem talál más magyarázatot, mint hogy a fény anyagi valami, amelynek flogiszton-tartalma van. A flogiszton általában valami elemféle, amely minden fontos vegyi változásnál egyik testből a másikba megy át. A flogiszton vegyületbe lép a tűzlevegővel is s ebből az egyesülésből lesz a fény és hő. A két utóbbi tehát anyagi természetű. Hogy ilyen téves felfogásokhoz jutott, annak főoka az volt, hogy vizsgálatai csak minőségi természetűek voltak, a mennyiségi viszonyokkal nem sokat törődött. Az ő felfogása szerint az égésterméknek könnyebbnek kell lennie, mint volt az elégett test és a fölvett oxigén együtt, mert hiszen a mérhető anyag egy részéből fény és hő lett, s ez eltávozott a testből. Az ő flogiszton-elmélete nem is talált követőkre, s az ellenfelek könnyen kivégezték. Stahl felfogása még egyszerűbb volt, nála az égés flogiszton kiválását és távozását jelentette; ugyanez Scheelénél már bomlás és egyesülés az égő testben. Így mégis valami átmenet a következő korszak felfogásához, amely az égést oxigénnel való egyesülésnek tekinti. Nagyon valószínű, hogyha Scheele nem hal meg olyan korán, éppen az általa fölfedezett új tények őt magát is átterelték volna a flogiszton-elmélet ellenzőinek táborába.
ÖTÖDIK FEJEZET
A MENNYISÉGI VIZSGÁLATOK KORSZAKA
»A természettudomány egyes ágaiban csak annyi a tulajdonképpeni tudomány, mint amennyi matematika van bennük.«
Kant
A flogiszton-korszak ideje alatt igen nagy fejlődésnek indult a kémia s a nagy, fontos gyakorlati felfedezések egymást érték. Ez egyrészt annak volt köszönhető, hogy az elmélet alapján, annak ellenére, hogy téves volt, bizonyos szisztematika szerint lehetett kutatni. Másrészt annak, hogy a XVIII. században találjuk a gépesített nagyipar kezdetét. Ekkor tökéletesedett a gőzgép James Watt (1736—1819) kezében annyira, hogy gépeket lehetett vele hajtani. S a gépek meg is jelentek, legelőször a textiliparban. Ennek nyomán a gyapotfeldolgozó üzemek gombamód szaporodtak. A gépeket kezdetben fából csinálták, később vasra tértek át. A vaskohászat azonban nem bírta a keresletet kielégíteni, hiszen a kohók faszenet használtak s az erdők fogytán voltak. Megpróbálták persze a kőszenet felhasználni, s ez hosszas kísérletezés után sikerült is. A kohóipar most tehát hatalmas fejlődésnek indult. Ez magával hozta, hogy új, megfelelő érceket kellett keresni. Ehhez pedig az analitikai kémia kellett. S valóban ebben a században alakult ki az analitika, először a minőségi s azután lassan a mennyiségi eljárás. Elsősorban a legfejlettebb vasiparú országokban fejlődött az analitika, Svédországban és Angliában. Különösen a svédek voltak kiválóak, ők vezették be a felbecsülhetetlen hasznosságú forrasztócsövet a minőségi vizsgálatokban. Páratlan szorgalommal elemezték a vegyészek a föld kőzeteit s természetszerűleg sok új, ismeretlen elemre bukkantak. Mennyiségi meghatározásokkal is próbálkoztak, s megszokták a mérleg használatát. Eközben, persze, óhatatlanul rábukkantak a flogiszton-elmélet ellentmondásaira. Miért növekszik a fémek súlya égéskor, ha flogiszton távozik belőlük? Mert tűzrészecskéket vesz fel — mondták Stahl nyomán. Megmérték hideg és izzó vas súlyát, de nem találtak köztük lényeges különbséget. Ez tehát nem áll! Persze, nagyon nehéz begyökeresedett elképzelésektől megszabadulni. Az ellentmondó jelenségeket először úgy próbálták magyarázni, hogy az elméletet módosítgatták. Legérdekesebb Guyton de Morveau egy elképzelése, amely szerint a flogiszton negatív súlyú, ha tehát ez távozik a fémekből, azok súlya több, ha egyesül velük, kevesebb lesz. Még kísérleti példával is megvilágította elképzelését. Tegyünk víz alá egy mérleget — írta — s mindkét karjára helyezzünk egyenlő súlyú ólomgolyócskát. Ezután helyezzünk az egyik karra egy parafadarabot, s ez a kar, annak ellenére, hogy hozzáadtunk valamit, mégis emelkedni fog. A parafa könnyebb a víznél, a flogiszton viszont könnyebb a levegőnél, levegőben mérve tehát a flogiszton-felvétel és -eltávozás teljesen analóg képet fog mutatni. Amikor Cavendish felfedezte a hidrogént, kialakult egy másik elképzelés. A hidrogén a flogiszton. A levegőnél könnyebb, szemmel láthatóan fémekből távozik el, ha azokat savban oldjuk, s ha fémoxidokhoz adjuk, azokból ennek hatására újra fém lesz. Ám Pierre Bayen (1725—1798) megfigyelte azt, hogy a higanyoxid hevítésre higannyá alakul (1772). A folyamat tehát épp ellentétes a flogiszton-elmélet tanításával. Most tehát már végképpen megvolt minden adat az új égéselmélethez s ezen keresztül az anyagmegmaradás elvéhez. Csak egy ember kellett, aki meg tudjon szabadulni agyában a flogiszton-elképzeléstől. Ez nem várathatott soká magára. Meg is tette Lavoisier. Bár már hallatszott előtte is egy távoli hang, Lomonoszov hangja, de amikor az övé szólt, még túl kevés volt az adat, meg túl halkan is hallatszott, semhogy hatása lett volna.
Amilyen gyorsan elterjedt hajdan a flogiszton-elmélet, olyan nehéz volt kiszorítani. Érdekes példája ez annak, hogy milyen nehéz az embereknek a beléjük gyökeresedett nézetektől megszabadulniuk. A tudósvilág kézzel-lábbal tiltakozott az új elmélet ellen, nyakatekertnél nyakatekertebb elgondolások születtek a flogiszton védelmében. Ehhez az ellenálláshoz az is hozzájárult, hogy az új elgondolás Franciaországból jött, ahol akkor volt a forradalom, s alaposan felforgatták a társadalom rendjét. S ezért más országokban akkor minden gyanús volt, ami onnan jött. Mennyi jó régi szokást félredobtak, s lám nem átallják a régi jó flogisztont is elvetni határtalan rombolási kedvükben! Jó lesz vigyázni evvel az új elgondolással! A kor legnagyobb vegyészei, a legtöbbje azoknak, akiket az előbbi oldalakon felsoroltunk, meg is halt úgy, hogy kitartott a flogiszton mellett. Mintegy 30 év, egy egész új nemzedék kellett hozzá, hogy Lavoisier elgondolásai általános elfogadásra találjanak. De amint ez megtörtént, páratlanul gyors fejlődésnek indult a kémia.
LOMONOSZOV
A XV—XVI. század szellemi fellendülésének hullámai Oroszországba csak a XVIII. században, nem kis mértékben I. Péter cár tudatos munkálkodása eredményeképpen érkeztek el. Az oroszországi tudományos fellendülés első nagy alakja bámulatosan sokoldalú, sok nyelvet beszélő férfi, aki a szellem- és természettudományok nem egy ágába véste bele kitörölhetetlenül a nevét. Ez az ember Mihail Vasziljevics Lomonoszov.
Lomonoszov először is költő volt, sőt az orosz költészetnek tulajdonképpeni megalapítója. Sok költeményt írt, többek közt egy eposzt is Nagy Péterről, továbbá két antik korban lejátszódó drámát. Tudatos nyelvújító és nyelvész volt. Történetíró volt: megírta a „Régi orosz történet”-et, az első orosz történelmi művet. Festő volt: több, jól sikerült festményét őrzik, legjobb közülük a „Poltavai csata” című. Értekezést írt „az orosz nép szaporodásáról”, s ezenkívül több egyházellenes vitairatot. Mozaikképeket rakott ki. Egy 4000 különböző üvegdarabból álló mozaikképet ajándékozott Erzsébet cárnőnek, aki ezért viszonzásképpen egy falut ajándékozott jobbágyokkal neki, hogy ott színesüveggyárat építhessen. Ez meg is történt, s Lomonoszov egyéb dolga mellett haláláig vezette is ezt a még ma is működő üzemet. Számos földrajzi, geológiai, meteorológiai és csillagászati tárgyú műve maradt még fenn. S mindemellett Lomonoszov meglepően éleslátású, előremutató vegyész is! Lomonoszovot, a természettudóst azonban sokáig eltakarta Lomonoszov, a költő és nyelvújító alakja. Halála után az orosz Akadémia és nyomában a társadalom elsősorban költőként méltatta. A régibb lexikonok pl. egy szóval sem említik azt, hogy Lomonoszov természettudós is volt. Igaz, hogy kémiai és fizikai gondolatainak egy részét akkoriban még meg sem értették, hisz sok tekintetben száz évvel előtte járt korának. Igaz az is, hogy Lomonoszov gondolatait, eredményeit gyakran csak kéziratos, befejezetlen formában hagyta, vagy elgondolásainak csupán vázlatát vetette papírra.
Így maradt meg például egy fizikai-kémiai könyvének tartalom-jegyzéke vagy számos előadásának emlékeztetőként leírt gondolatmenete.
Százötven évi méltatlan elfelejtés után, e század elején ásta elő Mensutkin, a neves orosz vegyész, Lomonoszov természettudományos tevékenységét az orosz akadémiai könyvtárnak mélyéből. E tevékenység a világ tudomására 1910-ben jutott, amikor Ostwald Lomonoszov egyes műveit kiadta a „Klassiker der exakten Naturwissenschaften’’ (Az exakt természettudományok klasszikusai) című sorozatában. Ennek a kiadásnak előszavában olvasható: »nagyon valószínű, hogy Lomonoszov Lavoisier korában és akkor, ha szellemi képességét kizárólag a kémiára koncentrálta volna, ugyanazt az eredményt, mint Lavoisier, elérte volna.”
Mihail Vasziljevics Lomonoszov 1711-ben született az Északi Jeges-tenger közelében, Gyeniszovka faluban, amely ma az ő nevét viseli. Jobbmódú parasztgyerek volt. Hatalmas kíváncsiság lakozhatott benne már gyerekkorában is, mert ebben a távoli faluban már egész fiatalon megtanult írni és olvasni. Hogy ezt hogyan érhette el az akkori orosz kulturális viszonyok között, amikor a falusi lakosság általában analfabéta volt, nem tudjuk megállapítani, valószínűleg autodidakta volt. Tizenkilenc éves korában elszökött a faluból, ahol addig apjának segédkezett, Moszkvába ment, és a szpaszki iskolába iratkozott be. Elég keserves volt a helyzete, egyrészt mert jóval idősebb volt iskolatársainál, akik ezért csúfolták, másrészt mert, ahogy később írta,
„ ... Tanulóéveim alatt a tudománytól eltaszító erők szorongattak. Egy felől apám, kinek egyetlen gyermeke voltam, azt vetette szememre, hogy én, egyetlen sarja, elhagytam őt és otthagytam azt a vagyont, melyet véres verejtékével szerzett nekem s melyet halála után majd idegenek prédáinak el. Másfelől a kimondhatatlan szegénység: naponta csak egy altinom volt, és így nem költhettem kosztra többet, mint félkopeket kenyérre és félkopeket kvaszra, a többi papírra, lábbelire és egyéb szükségesre ment el. Így éltem öt évig, de a tudományt mégsem hagytam ott!”
Nagy szerencse érte 1735-ben. A kormány leírt az iskolába, hogy a legtehetségesebb diákokat küldjék az akadémiára tanulni, e Lomonoszov a kiválasztottak közé tartozott. Lomonoszov az akadémián természettudományokkal foglalkozott és annyira tehetségesnek mutatkozott, hogy már a következő évben két társával együtt nyugat-európai tanumányútra küldték. Először Marburgban töltöttek egy évet Christian Wolff, a neves Leibnitz tanítványa s mint ilyen, teleológista filozófus és fizikus mellett, aki az orosz Akadémia tiszteletbeli tagja volt. Innen a freibergi bányászati akadémiára mentek Henckel mellé analitikai és kohászati tanulmányok végzésére. Míg Wolffról Lomonoszov mindig nagy véleménnyel volt, Henckel tudását nem értékelte túl sokra. Freibergben is egy évet töltöttek, majd tovább vándoroltak s beutazták Németországot és Hollandiát. Lomonoszov ezután visszatért Marburgba, ahol meg is nősült.
1741-ben, ötévi távollét után érkezett vissza Pétervárra. Elkészített egy disszertációt, amely nem maradt fenn, s ezután a fizikai osztály adjunktusává nevezték ki (1742). Ő volt az első, aki előadásait orosz nyelven tartotta. Az Akadémiára Péter cár akkoriban neves külföldi tudósokat hívott meg. Ez a szokás utána is megmaradt, csak annyi változással, hogy egyre kevésbé nevesek voltak azok, akik hajlandók voltak elfogadni a meghívást a Nagy Pétert követő zavaros oroszországi körülmények közé. Az akadémia vezetése Lomonoszov idejében egy ilyen kisebbhírű német klikk kezében volt, s a fiatal adjunktus csakhamar ellentétbe került velük. Ezt heves természete csak fokozta. Mikor egy ízben a földrajz professzorát és a többi német tudóst röviden „hunefutoknak és kurafiaknak” nevezte, azok bepanaszolták, s Lomonoszovot félévre lecsukták, de aztán Szuvolov gróf, Erzsébet cárnő kegyencének közbenjárására kiengedték, azzal a feltétellel, hogy bocsánatot kér a megsértett akadémikusoktól.
1745-ben Lomonoszov a kémia professzora lett. Az ezt követő tíz év Lomonoszov kémiai kutatásai szempontjából a legértékesebb. Ez idő alatt rendezte be az első korszerű laboratóriumot Oroszországban. Harcolt azért, hogy Oroszországban egyetemet állítsanak fel, mégpedig egy, az állam és klérus beavatkozásának ki nem tett, autonómiával felruházott egyetemet. Harca sikerrel járt, 1755-ben meg is alakult a moszkvai egyetem, amely ma Lomonoszov nevét viseli. 1756-ban lemondott kémia professzoriságáról, mert az akadémia titkára s a gimnázium igazgatója lett. Pártfogója, Szuvolov nála tanult poétikát, s állandóan arra akarta rábírni, hagyja abba a természettudományokat, hiszen a költészet és történelem az igazi területe. Valóban, ezentúl egyre kevésbé foglalkozott kémiával, bár néha-néha még visszatért hozzá. Már saját házában is volt laboratóriuma, amelyben néha még kísérletezett. A túlfeszített munka felőrölte Lomonoszovot, s idő előtt hunyt el hosszas betegség után, 1765-ben.
„Nyugodtan halok meg, csak azt sajnálom, hogy nem fejezhettem be mindazt, amit a haza javára, a tudományok fejlesztésére és az Akadémia dicsőségére elkezdettem s most életem végén azt kell látnom, hogy velem együtt odalesz minden hasznos szándékom” — mondotta Lomonoszov halálos ágyán, s bizony sok tekintetben igazolódott megérzése!
A kémia és fizika területéről legérdekesebb Lomonoszov egy értekezése a "legkisebb észrevehetetlen fizikai részecskékről, melyekből a természetes testek állanak". Ebből kiderül, hogy a testeket atomisztikus felépítésűeknek tartotta. A testek kicsi, észre nem vehető részecskékből állanak, amelyek körmozgásban vannak, s amelyeknek határozott alakjuk és térfogatuk van. Különböző anyagok atomjai különböző alakúak. Érdekes Lomonoszov elgondolása a levegőről! Mintha már a kinetikus gázelmélet villant volna fel előtte. A levegő atomjai nem érintkeznek közvetlenül egymással, különben a levegő nem lenne összenyomható. Mozgásuk révén viszont ütköznek egymással, s az ütközések folytán szerteszóródnak, ettől származik a levegő rugalmassága. Minél erősebben nyomjuk össze a levegőt, annál többször ütköznek össze az atomok, a levegő rugalmassága tehát nő. A levegő sűrűsége nagy nyomáson azonban nem arányos rugalmasságával, mert ilyenkor már tekintetbe kell venni az atomok saját térfogatát is! A hőmérséklet az atomok mozgásának gyorsaságától függ. A szilárd test atomjai csak körmozgást végezhetnek, mert kohézió tartja őket össze. A meleg test atomjai gyorsabban mozognak a hidegénél, minél gyorsabbá válik a mozgás, annál jobban feszül a kohézió, végül ez elszakad és a test megolvad.
„Ahogy az atomok mozgási gyorsaságának határait nem lehet elképzelni, akképpen a meleg felső határát sem lehet. Az ellenkező irányban azonban elképzelhető, hogy a mozgás teljesen megszűnik. A hidegnek legvégső foka eszerint a hőmozgás teljes megszűnése, és ez az állapot létezhet” (!)
Látható, hogy Lomonoszov a jelenségeknek fizikai-mechanikai értelmezését keresi mindig, s ez ebben a században még teljesen szokatlan!
Lomonoszov tudatosan kereste a kémiai -jelenségek fizikai magyarázatát. Fizikai kémia címen is hirdet előadásokat.
„A fizikai kémia az a tudomány, amely a fizika tételei és kísérletei alapján megmagyarázza azt, ami a vegyületekben kémiai műveletek által történik. Nevezhető lenne ez kémiai filozófiának is, de egészen más értelemben, mint az a misztikus filozófia, amely nemcsak hogy nem ad magyarázatokat, hanem még magukat a műveleteket is titokban hajtja végre” — írja.
Megmaradt fizikai kémia tárgyú kutatásainak egy tervezett programja. Eszerint oldhatóságvizsgálattal s ennek hőmérsékletfüggésével kívánt foglalkozni, azután folyadékok hőmérsékletváltozás okozta térfogatváltozásával, oldatok forrás- és fagyáspontjának megállapításával, a fény törésével oldatokban, stb. Ez a gazdag program azonban többnyire csak papír maradt. Legalábbis vizsgálatok nyoma kevés, valószínűleg sorra se kerültek! Csupán a vegyületek oldhatósági vizsgálatairól maradtak eredmények. Közönséges hőmérsékleten Lomonoszov e mérései elég pontosnak bizonyultak, magas hőfokon azonban általában jóval kisebbek értékei a maiaknál.
Lomonoszov megismételte Robert Boyle híres kísérletét is. Boyle ui. ónt égetett el zárt edényben, s megállapította, hogy a rendszer súlya növekedett. A jelenséget tűzrészecskék felvételével magyarázta. A téves észlelés feltehetően onnan származott, hogy Boyle mérés előtt kinyithatta az edényt és abba levegő tódult. Lomonoszov megállapította, hogy Boyle mérése hibás volt és hogy az anyagok összsúlya változatlan maradt.
Már ekkor gondolt arra, hogy nyitott rendszerben elégetve fémet, az észlelhető súlyszaporulat nem a levegő adszorpciójából származik-e.
Mindezt Lomonoszov azonban megint csak futólag említi meg 1756. évi akadémiai beszámolójában, célozva arra, hogy a kérdésről részletes beszámolót fog írni, ami azonban, úgy látszik, elmaradt. Érdekes Lomonoszov egy levele, amelyet 1748-ban Euler-hez, a nagy matematikushoz írt. Ebben a következőket olvashatjuk: »Minden változás a természetben úgy történik, hogy ha valami valamihez hozzáadódik, az másutt ugyanolyan mértékben csökken. Ha tehát egy test anyaga növekszik, valamely másik testé ugyanannyit csökken. A természet e törvénye általános, és a mozgásnál is alkalmazható: ha egy test a maga lökésével mozgásba hoz egy másikat, ugyanannyit veszít a maga mozgásából, mint amennyit a másiknak átadott.«
Ez voltaképpen az energia- és anyagmegmaradás elvének szabatos, bár kísérletileg és matematikailag nem bizonyított kifejtése. Valószínű, hogy a következő években kísérleti adatokat gyűjtött ez állításához, mert csak 1760-ban adta elő tételét nyilvánosan egy előadásában, mely túl sok figyelmet nem kelthetett, mert halála után 1778-ban az Akadémia által kiadott gyűjteményes műveiből ez az előadás már hiányzik.
Az anyagmegmaradás elvét Boyle égetési kísérletének újabb megismétlése alapján 13 évvel Lomonoszov halála után állapította meg újra Lavoisier, az energiamegmaradás elve és a fizikai kémia még száz évig várattak magukra. Ha nem foglalkozott volna annyi mindennel Lomonoszov, hanem csak kémiával, ha gondolatait, eredményeit, kísérleteit valahol összefüggően, fegyelmezetten rendszerezte és leírta volna, akkor talán ma nevéhez fűződne a modern kémia megteremtésének dicsősége. Így azonban ez a szerep Lavoisiernek jutott.
LAVOISIER
Antoine-Laurent Lavoisier francia kispolgári családból származott. Legrégibb ismert őse Antoine Lavoisier postakocsis volt, aki 1620-ban halt meg. Lavoisier apja már többre vitte: postamester, ügyész, majd ügyvéd volt; a XVIII. század közepe táján Párizsba költözött és szépen megszedte magát. Az apa
1742-ben házasodott meg, s a következő évben, augusztus 26-án született meg a mi nagy vegyészünk; aztán még egy nővére született. Ötéves korában elvesztette anyját, majd tizenkét év múlva a nővérét is. Apja és nagynénje nevelték. Szorgalmas, munkaszerető fiú volt, iskola évei simán teltek el. 1760-ban nagy díjat kapott egy szónoki versenyen. Tehát mint oly sok tudósnál láttuk, ő is klasszikus tanulmányokkal kezdte meg pályáját, vidéki akadémiák kitűzött díjaira pályázva. 1764-ben parlamenti ügyvéd lett. De hajlama a természettudomány felé vonzotta, előbb általánosságban, csillagászat, növénytan, ásványtan, vegytan egyformán érdekelte. Itt-ott társadalmi problémákkal, közgazdaságtannal is foglalkozott.
Húszéves korában szeretett volna már valami önálló kutatást végezni. Akkor meteorológiai és barométeres megfigyelésekre vetette magát, amit egész életén át folytatott, bár későbben mérsékelten, mert szerette volna fölfedezni a légköri mozgások általános törvényét.
1765-ben a francia Akadémia díjat tűzött ki arra a kérdésre, mi lenne a legjobb módja nagyvárosok éjjeli megvilágításának. Lavoisier is pályázott. De hogy ne csupán a kisujjából szopja a választ, állítólag hat hétre bezárkózott egy sötét szobába, s ott tanulmányozta a különféle lámpák világítóképességét, fényerejét. Sajnos, egyik forrásban se találjuk, mi volt az ő válasza a pályakérdésre, csak annyit tudunk, hogy nem kapta meg a pályadíjat, hanem aranyéremmel honorálták. Más forrás szerint igenis neki ítélték a kétezer frankos díjat, de ő ezt nem akarta elvonni a szegényebb pályázóktól, nekik engedte át, s így kárpótolták aranyéremmel, az akadémiának 1766-ban tartott nyilvános ülésén.
Ugyanebben az időben Guettard nevű mesterének segédkezett Franciaország ásványtani térképének elkészítésében, ezért mesterével együtt beutazta hazájának hegyes részeit. Ez volt Franciaország első geológiai térképe. E térkép elkészítéséhez ásvány-vegytani vizsgálatokat is kellett végezni, s Lavoisier ekkor végezte első vegytani kutatását a Párizs környéki gipszeken. Ez a munkája, huszonkét éves korában, 1765-ben jelent meg. Ettől kezdve egymás után jelentek meg dolgozatai más tárgyakról, a mennydörgésről, a sarki fényről, a víz megfagyásáról stb. Neve ismeretessé vált tudós körökben, az Akadémia 1768-ban megválasztotta másodrendű tagjának (mint nálunk a levelező tag). A híres Lalande csillagász későbben följegyezte, hogy ő is támogatta a kinevezését, mert úgy gondolta, hogy »a tudomány nagy hasznát veheti égy olyan tudós, eszes, fürge fiatalembernek, akit a sors más pályára ragadhatna«. Lavoisier tehát már egészen fiatalon bekapcsolódott az Akadémia munkájába, mert akkoriban a tagság nem egyszerű dísz volt, a tagoknak dolgozniuk is kellett. Szívesen is vállalt minden munkát, egyik legszorgalmasabb tagja lett a nagytekintélyű testületnek. Az üléseken sok dolgozatát olvasták föl a legkülönbözőbb tárgyakról. De ekkor még semmi sem mutatta, hogy lángelméje valamilyen határozott irányba terelődött volna.
Ebben az időben anyagi természetű vágyai támadtak: szerette volna nemcsak megkímélni, hanem meg is növelni anyjától örökölt vagyonát. Egy hónappal azután, hogy tagja lett az Akadémiának, belépett az Adóbérlők Társaságába (Ferme Général), amely a kormánytól az adók behajtását bérelte, 1779-től nagy szerepet játszott ennél a társaságnál, egészen 1791-ig, amikor a nemzetgyűlés megszüntette az intézményt. Ez a működése tekintélyes vagyont hozott néki. De nagy buzgalommal foglalkozott sok egyébbel is. 1775-ben megbízták a puskaporgyártás vezetésével. Itt sok hasznos reformot valósított meg vegytani ismeretei révén. De foglalkozott a mezőgazdaság egyes fontos problémáival is, indítványozta a burgonya- és lentermelés meghonosítását, tudományos tanácsokat adott a répatermeléshez és juhtenyésztéshez. Állandó levelezésben volt a miniszterekkel, akik gyakran kértek tőle tudományos szakértői véleményt. 1787-ben az ő javaslatára vették körül fallal Párizst, amely eljárás népszerűtlensége ebben az akkori szójátékban fejeződött ki: »Le mur murant Paris, rend Paris murmurant.« (Szó szerint: A Párizst övező fal miatt Párizs morog.) Ehhez járult még a saját tekintélyes birtokának igazgatása (1778-ban vásárolta); ott állandóan érdekes mezőgazdasági kísérleteket végzett.
Ez igazán sokféle elfoglaltság volt, de ő győzte energiával. Minden rábízott közügyet lelkiismeretesen végzett, mégis módját ejtette, hogy napi hat órát szenteljen a tudománynak. Az tette lehetővé ezt, hogy az adóbérletből eredő nagy jövedelme anyagi függetlenséget biztosított neki. Igaz, hogy ugyanez az adóbérlet okozta halálát. Egyes akadémiai tagtársai, talán szintén irigységből, úgy nyilatkoztak ugyan, hogy a gazdagság nem egyeztethető össze a tudományos munkálkodással, de más tagok azt mondták erre: »Annál jobb ebédeket kapunk tőle!« Ezek az ebédek valóban híresek voltak.
Hetenként egy napot kizárólag tudományos kutatásoknak szentelt. Felesége ezt írta erről: »A boldogság napja volt ez számára; már reggel összeült a laboratóriumban néhány kiváló barátja, néhány fiatalember, akik büszkék voltak a megtiszteltetésre, hogy segítségére lehetnek a kísérletezéseinél. Ott reggeliztek, ott vitatkoztak; ott alakították ki azt az elméletet, amely halhatatlanná tette a szerzőjét."
Mikor 1775-ben kinevezték a lőporgyártás felügyelőjének, az arzenálban rendezte be a laboratóriumát, s ott dolgozott 1792-ig, amikor megfosztották ettől a tisztségétől. Ez a laboratórium tizenhét éven át volt színhelye a szakadatlan munkának. Nemcsak a saját önálló kutatásait végezte, hanem sok időt szentelt annak, hogy megismételje más tudósok kísérleteit, ha hírt kapott ezekről, például Black kísérleteit a szénsavval, Priestley kísérleteit az új gázzal, Cavendish kísérleteit a vízzel és salétromsavval. Mindig kiváló szaktudósokat hívott meg s ezek előtt ismételte meg ezeket a kísérleteket. A meghívottak között szerepeltek olyan nevek, mint Macquer, Baumé, Darcet, Guyton de Morveau, Lagrange, Laplace, Berthollet, Fourcroy stb. Tehát úgyszólván a tudós-nyilvánosság előtt végezte a kísérleteit, mindig a legújabb és legjobb műszerek, penumatikus kádak, hőmérők, mérlegek stb. fölhasználásával. Azt mondják, hogy pusztán a víz összetétele az alkatrészeiből körülbelül 50 000 frankjába került Lavoisiernek (ma középiskolai vegytanóra keretében is bemutatják ezt, nem kerül semmibe).
Lavoisier háza szinte a tudományos központja volt Párizsnak. Sok külföldi tudóssal állott levelezésben, ami hasznos szokás volt abban az időben, s ha ezek a tudósok elkerültek Párizsba, okvetlenül meglátogatták nagy kollégájukat. Így olvastuk a Priestley könyvéből közölt szövegben, hogy Priestley is fölkereste; járt nála James Watt, Benjamin Franklin stb.
1791-ben az Akadémia pénztárosa lett, ugyanakkor tagja annak a bizottságnak, amelynek föladata volt új egységes mértékrendszert megállapítani: a méter-rendszert. 1792-ben Lavoisier és Haüy határozta meg a desztillált víz sűrűségét, ami alapja lett a súlyegységnek, a kilogrammnak. A következő évben megint csak Lavoisier mérte meg Borda-val együtt a réz és a platina viszonylagos kiterjedését, hogy így létrehozzák a méter ősmintáját.
Minthogy Lavoisier személyét kizárólag kémiatörténeti szempontból és kémiai oldalról világították meg az utókorban és emellett közéleti, politikai szereplését egyáltalán nem vizsgálták, erről nem is igen tudunk, úgyhogy nem tudjuk megítélni, mennyire volt indokolt vagy indokolatlan az ellene folytatott közismert per és ítélet. Tény az, hogy 1794-ben, több más adóbérlővel együtt őt is perbefogták, halálra ítélték, s az ítéletet május 8-án végrehajtották rajta.
Lavoisier emberi jellemét a különböző források különbözőképp ítélik meg. A franciák égig magasztalják. A külföldiek, különösen a német források, sok minden kevésbé épületest írnak róla. Ha a kortársak véleményét is nézzük, egy kétségtelen: Lavoisier zsenialitásánál csak hiúsága és dicsőségvágya volt nagyobb. Bár saját felfedezései forradalmat idéztek elő a kémiában, idegen eredményeket is szeretett sajátjaként közölni. Tudományos működését állandó prioritás viták kísérik. Kora minden nagy vegyésze, Bergman, Black, Cavendish,. Marggraf, Priestley többé-kevésbé neheztel rá ilyesmik miatt. S maga Lavoisier is gyakran mosakszik utólag, hogy „elfelejtette megemlíteni”, hogy nem eredeti kísérletét mutat be. A francia Akadémia őriz 40 g vizet, amelyet Lavoisier állított elő hidrogénből és oxigénből anélkül, hogy Cavendisht említette volna. Priestley méltatlankodását az oxigén felfedezésével kapcsolatban már említettük, s Lavoisier helyesbített is "meglehet, hogy Priestley úr tőlem függetlenül már valamivel előbb rájött..." stb.
Mindazonáltal nem vitatható, hogy a modern kémia megalapítása Lavoisier nevéhez fűződik. Tárgyilagosság kedvéért jegyezzük meg, Priestley és Cavendish meg a többiek felfedezéseinek jelentősége is csak Lavoisier kezében mutatkozott meg igazán.
Lavoisiernek csaknem minden írása a párizsi Akadémia évkönyveiben jelent meg, 1768 és 1787 között körülbelül hatvan értekezés. Aki azonban az akadémiai évkönyv dátumai alapján akarná megállapítani az egyes fölfedezéseinek keltét, az súlyos tévedéseket követne el, mert az egy-egy évben benyújtott dolgozatok majdnem mindig három évvel későbben jelentek meg, hiszen abban a korban semmi sem volt sürgős. Például Lavoisier 1782-ben írta meg dolgozatát az oxidok összetételéről, de ez csak 1785-ben jelent meg. Viszont megtörtént az ellenkező furcsaság is: 1783-ban végezte a víz összetételére vonatkozó kísérleteit, 1784-ben terjesztette az eredményeit az Akadémia elé s ez mégis 1781-es keltezéssel jelent meg! Ezenkívül közleményei jelentek meg az »Annales de chimie«-ben, a »Journal de Physique«-ben, az »Academ,ie de médécine«-ben. Éppen élete utolsó évében foglalkozott a gondolattal, hogy kiadja összegyűjtött munkáit, de csak halála után, 1805-ben került a sor erre. 1789-ben megjelent egy nagyobb munkája, amelyben összefoglalóan ismerteti a fölfogását: »Traité élémentaire de chymie, présenté dans un ordre nouveau et d’aprés les découverts modernes" (Elemi vegytan, új rendszerben és a legújabb fölfedezések alapján). Halála előtt ezt kezdte átdolgozni, új kiadásra elkészítve. Ennek a könyvének legjellemzőbb vonása volt az addig szokatlan világosság és következetesség, amellyel ismertette a vegytan legfontosabb tényeit; lefordították német és angol nyelvre is, szinte bibliája volt az új vegytannak.
*
Lavoisier egész munkásságának legjellemzőbb vonása a megfigyelések alapossága, leírásuk szabatossága és a minden dogma nélküli, elfogulatlan következtetés. Alaposságának és következetességének irányítója a mérleg. De itt egy tévedést kell helyreigazítanunk. Általános a fölfogás, hogy Lavoisier vezette be a mérleget a vegytani vizsgálati eszközök közé. Ez semmiképpen nem áll. Mint Blacknél, Cavendishnél és Bergmannál láttuk, már ők is használták a mérleget. De igenis Lavoisier érdeme, hogy a vegyi átalakulásoknál a mérleget tette meg döntőbírónak, az átalakulás minden termékének lehelő legpontosabb megmérését, nem csupán a folyékony vagy szilárd, hanem a gáz alakú termékek megmérését is ő vezette be. Így felelt meg ösztönszerűen annak a kanti követelménynek — bár még nem is ismerhette Kantot — amelyet e fejezet elejére tettünk jelszónak. Így tudta elérni, hogy bármely elődjénél sokkal pontosabban látta a vegytani tényeket, s így elméletileg is pontosabban és átfogóbban értelmezhette őket. Ez utóbbi elmemunkánál nagy segítségére volt széleskörű tudása: mindenről tudott, ami előtte történt a vegytani kutatások terén, tehát ismerte a problémák történeti fejlődésért is. Van egy vezérgondolata, amely szinte minden kutatását összekapcsolja: az égés és a fémek elmeszesedésének mibenléte, s mikor megoldja ezt a titkot az oxigénnel, akkor ennek az elemnek szerepét keresi a legtöbb vegyi átalakulásnál. Ez az oxigén-kutatása olyan alapos, módszerében is olyan tökéletes volt, hogy későbben mintául szolgált másoknak más elemek kutatásánál is.
Lavoisier nem vaktában, hanem tervszerűen kutatta az égésjelenség mibenlétét, előre kitűzött céllal: meg volt győződve a flogiszton-elmélet helytelenségéről, jobbat akart tenni a helyébe, de nem spekulatív alapon, hanem kísérletileg bizonyított tények alapján. Az eszme 1772 őszén fogamzott meg benne, leírta ezt a tervét meg az első kísérleteit, s az okmányt zárt borítékban átadta az Akadémia titkárának 1772. november 1-én, de csak a következő év májusában bontották föl. Ránkmaradt laboratóriumi följegyzéseiben 1772. szeptember 10. az első dátum. A letétbe helyezett okmányban előadja, hogy fémek elmeszesedésénél, továbbá foszfor vagy kén elégetésénél súlygyarapodás áll elő, aminek oka levegőelnyelés; viszont fém-mész redukálásánál nagy mennyiségű levegő (gáz) szabadul föl.
1774-ben hozza nyilvánosságra a kísérleteit. Boyle nyomán indul el: ónt tesz edénybe, ezt hermetikusan elzárja és megméri az egészet; hevítéssel az ón elmeszesedik. Akkor újból megméri az egész rendszert, s változatlannak találja a súlyt. Itt eltér Boyletól, aki súlygyarapodást vélt észlelni. Mikor Lavoisier kinyitotta a retortát, levegő tódult be, és most már súlygyarapodás állott elő, mert a rendszer nehezebb lett a betódult levegő súlyával; ha kivette az elmeszesedett ónt, ez pontosan annyival mutatkozott súlyosabbnak, mint amennyi volt a betódult levegő súlya. Az elmeszesedés tehát abban áll, hogy a fém levegőt vesz föl, vagy ennek valamilyen alkatrészét. Az égésnek lényege tehát sehogyan sem lehet flogiszton eltávozása, mint eddig gondolták. A foszfor vagy a kén elégetésénél tökéletesen ugyanezt tapasztalta: tehát a fémek elmeszesedése és a savak keletkezése teljesen azonos folyamat.
Lavoisier ekkor még nem tud az oxigénről, csak a levegő egyik alkatrészéről beszél, egészen bizonytalanul »fluide élastique«-nek nevezve ezt. Azonban kapóra jött egy szerencsés, véletlen. A Priestley könyvéből közölt hosszú idézetünkben benne van az a rész is, ahol Priestley megemlíti Lavoisier-nál tett látogatását 1774 őszén. A közlékeny angol tudós elmondja neki fölfedezését az égést tápláló új gázzal. A francia tudós elméjében megvillan valami, tudomásul veszi a közlést, és forradalmat csinál a látszólag mellékes fölfedezésből. Így esett meg az a szépséghiba, hogy mikor későbben Lavoisier leírja azokat a kísérleteit, amelyek az oxigén fölfedezéséhez vezették, egy szóval sem említi Priestleyt, úgy tesz, mintha a fölfedezés teljesen az ő érdeme volna. Mikor nemsokára az angol tudós reklamálja az elsőséget, Lavoisier csak annyit ismer el, hogy egyidejűleg történt a fölfedezés. Pedig ma még a franciák is elismerik, hogy a fölfedezés elsősége Priestleyé. Ha Priestleyt nem tette volna annyira elfogódottá a flogiszton-elmélet, ha az általa fölfedezett új gázt nem nevezte volna deflogisztizált levegőnek, hanem valóban új gázt látott volna benne, ő lehetett volna elindítója annak az új korszaknak, amely így Lavoisier nevéhez kapcsolódott.
Priestley látogatása, illetve amit hallott tőle, lázas izgalomba hozta Lavoisiert. Rögtön újból kísérletezéshez fogott, most már még határozottabb célkitűzéssel. Ezek eredményeként ő már nem a levegő kétféle módosulását találta meg, a flogisztocizált és deflogisztizált levegőt, hanem rájött, hogy a légköri levegő két lényegesen eltérő alkatrészből áll: a fémek meszesedését okozó, az égést tápláló és lélegzésre alkalmas tiszta vagy éltető levegőből (amelyet későbben nevezett el oxigénnek), meg egy általa mofette-nek nevezett részből, amely nem táplálja a tüzet, lélegzésre alkalmatlan. De a flogisztonnak semmi köze az egészhez, ez csak elképzelt valami. Ezek a megállapítások teszik Lavoisier fölfedezésének lényegét, s ezekkel az első időkben szinte megbolondította a vegyészek világát. A flogiszton-elméletnek még mindig nagyszámú hívei annyira fölháborodtak, hogy például Berlinben »in effigie« máglyán égették el Lavoisiert- mint a tudomány eretnekét. De az általa föltárt tények annyira cáfolhatatlanok voltak, hogy a vegyészek elfogulatlan része rögtön elejtette a flogiszton-elméletet; nem mondhatnánk, hogy ezek voltak többségben.
De mutassuk be Lavoisier levegőelemzési kísérletét a saját szavaival (Traité élémentaire de chimie, I. köt. 3. fejezet):
»Azt állíthatjuk légkörünkről, hogy mindazon anyagok elegyéből kell állania. amelyek közepes hőmérsékleti és nyomásviszonyok mellett gázállapotban vannak. Ezek a gázok majdnem azonos összetételű tömeget képeznek a legnagyobb magasságokig, ameddig eddigelé fölszállottak. Sűrűségük egyenes arányban csökken a rájuk nehezedő súllyal.
Most meg akarjuk állapítani azoknak a gázoknak számát és természetét, amelyek a bennünket körülvevő réteget alkotják. A kísérlet világosítson föl bennünket erről. Általánosságban a vegytan két eszközt ad a kezünkbe egy anyag összetételének megállapítására, a szintézist és analízist. Vegytani téren nem is szabad megelégednünk addig, amíg nem egyesítettük a vizsgálatnak ezt a két módját.
Evvel az előnnyel szolgál a légköri levegő vizsgálata; föl lehet bontani és ismét összetenni. Én pedig arra fogok szorítkozni, hogy bemutassam itt az erre vonatkozólag végzett legfontosabb kísérleteket. Alig akad közöttük olyan, amely ne tőlem eredne, legföljebb új szempontból ismétlem meg. mégpedig a légköri levegő összetételével kapcsolatban.
Elővettem egy lombikot (lásd az ábrát) körülbelül 36 köbhüvelyk térfogattal, amelynek BCDE nyaka nagyon hosszú volt. Meghajlítottam úgy, amint a mellette levő ábrán látható, hogy bele lehetett helyezni az MMNN kemencébe, míg E vége áz FG burába torkollott, ez pedig az RE, higanykádba merült. Ebbe a lombikba négy uncia nagyon tiszta higanyt tettem. Azután lopót vezettem be az FG harang alá, megszívtam, mire a higany LL-ig emelkedett; enyvezett papírcsíkkal gondosan megjelöltem ezt a szintet, s pontosan megfigyeltem a barométerállást és a hőmérsékletet.
Elvégezvén ezeket az előkészületeket, tüzet gyújtottam a kemencében, ezt csaknem szakadatlanul égettem tizenkét napon át, úgyhogy a higany a forráspontjáig hevült fel.
Az egész első nap folyamán nem történt semmi lényeges. A higany nem forrt ugyan, mégis az állandó párolgás állapotában volt. Az edények belsejét cseppecskékkel vonta be, amelyek eleinte nagyon finomak voltak, lassanként nagyobbak lettek, és ha bizonyos nagyságot elértek, maguktól visszahullottak az edény fenekére, hogy egyesüljenek a többi higannyal. A második napon láttam, amint apró vörös foltocskák léptek föl a higany felületén, amelyek négy-öt napon át gyarapodtak számban és nagyságban. Akkor abbahagyták a növekedést, és teljesen abban az állapotban maradtak meg. Mikor 12 nap múlva úgy láttam, hogy a higany elmeszesedése egyáltalán nem halad többé előre, engedtem, hogy a tűz elaludjon és az edények kihűljenek. A kísérlet előtt annak az egész levegőnek a térfogata, amely a lombikban és a bura alatt volt, körülbelül 50 köbhüvelyk volt 28 hüvelyk nyomásra és 100 hőmérsékletre redukálva. A kísérlet befejezése után ugyanolyan hőmérsékleti és nyomásviszonyok mellett már csak 42—43 köbhüvelyk volt. A térfogat tehát körülbelül egyhatodával csökkent. Erre gondosan összegyűjtöttem a képződött vörös tömeget, és amennyire lehetett, megszabadítottam a higanytól. A súlya 445 szemer volt.
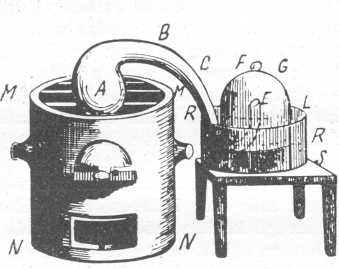
Lavoisier elemzi a légköri levegőt, elzárt levegőben higanyt hevít.
Az a levegő, amely e kísérlet után visszamaradt és amely eredeti térfogatának 5/6-ára csökkent, se lélegzéshez, se égéshez nem bizonyult alkalmasnak. A beletett állatok néhány pillanat múlva elpusztultak, a gyertya rögtön elaludt benne, mintha vízbe mártották volna.
Ezután nagyon kicsi üvegretortába tettem bele azt a 45 szemer vörös anyagot, amely a kísérlet folyamán képződött. A retortát összekapcsoltam alkalmas készülékkel az esetleges folyékony és gáz alakú termékek felfogására.
Miután tüzet gyújtottam a kemencében, megfigyeltem, hogy abban a mértékben, amint a vörös anyag melegedett, a színe sötétebb lett. Amint aztán a retorta közeledett az izzáshoz, a vörös anyag térfogata csökkenni kezdett, s néhány perc múlva egészen eltűnt.
Egyidejűleg a kis felfogóban 41 és 1/2 szemernyi folyékony higany sűrűsödött meg, a bura alatt pedig 7—8 köbhüvelyknyi olyan gáz lépett föl, amely a légköri levegőnél sokkal alkalmasabb volt az égés és lélegzés táplálásához. Miután ennek a gáznak egy részét egy 1 hüvelyk átmérőjű üvegcsőbe töltöttem és gyertyát tartottam belé, kápráztató fénnyel égett benne; a szén nem nyugodtan parázslott benne, mint a rendes levegőben, hanem olyan élénk fénnyel égett, hogy a szem alig tudta elviselni. Ezt a gázt, amelyet Priestley, Scheele és én majdnem egyidejűleg fedeztünk föl, az előbbi deflogisztizált levegőnek nevezte, a második tűzlevegőnek; én az oxigén nevet adom neki, mert egyik legfontosabb tulajdonsága, hogy savakat képez, miközben a legtöbb anyaggal egyesül. Ha elgondolkodunk ennek a kísérletnek körülményein, rájövünk, hogy miközben a higany elmeszesedik, fölveszi a levegőnek lélegzésre alkalmas részét, és hogy a levegőnek megmaradó része alkalmatlan az égés és lélegzés táplálására. Tehát a légköri levegő két különböző, majdnem azt mondanánk, ellentétes természetű gázból van összetéve.
Ennek a fontos igazságnak egyik próbája a következő: Ha ismét egyesítjük a két gázt, mégpedig 42 köbhüvelyk fojtógázt és 8 köbhüvelyk oxigént, olyan gázt kapunk, amely minden tekintetben megegyezik a légköri levegővel, és ugyanolyan mértékben alkalmas, az égésre, lélegzésre és a fémek elmeszesítésére.«
Lavoisier nem pihent meg a babérain, fáradhatatlanul szaporította a bizonyítékokat. Kimutatta, hogy a fix levegő (szénsav) sem egyéb, mint szén vegyülete oxigénnel, mert ha fém-meszet szénnel hevítenek, színfémet kapunk, a fém-mész másik alkatrésze a szénnel együtt fix levegővé alakul át. Még meggyőzőbb bizonyítékkal szolgál erről, mikor 1772—-73-ban gyémántot éget el oxigénben, s tiszta fix levegőt kap égéstermékül. Addig nem is tudták, mi a gyémánt, most már világos volt, hogy tiszta szén. Régebben is észlelték, hogy erős hő hatására a gyémánt eltűnik, de úgy vélték, hogy egyszerűen elpárolog; most már bizonyos volt, hogy elég. Lavoisier nagy üvegedényekben égette el a gyémántot, amelyeket vagy légköri levegővel vagy oxigénnel töltött meg, az elégetéshez nagy gyújtóüveget használt. Későbben rájött, hogy ugyanígy fix levegő keletkezik akkor is, ha gyémánt helyett közönséges faszenet éget el.
Ezen az alapon tovább dolgozva, Lavoisier tökéletesen fölforgatta a savak klasszikus fölfogását is. Megvizsgálta a foszfor és kén égését, s kimutatja, hogy ezeknek oxigénnel való egyesüléséből keletkezik a foszforsav és kénsav. A flogisztonnak megint csak semmi köze ehhez, nem igaz a régieknek az a fölfogása a kénről, hogy ez áll kénsavból és flogisztonból. Ez a megállapítás egyszerre fényt vetett a savak összetételére általában: ezekhez a savakhoz a fölfedezett tiszta levegő kell. Lavoisier megtalálta az alkalmas nevet is: oxigénnek (görögül «-savnemző«) nevezte el. A savak keletkezésének mennyiségi ellenőrzése megerősítette a fölfogását. Ha gyújtólencse segítségével foszfort égetett el zárt térben, levegő jelenlétében, a keletkezett fehér pelyhek (szilárd foszforsav) mindig a foszfor eredeti súlyának két és félszeresét tették, ami teljesen megfelelt az elnyelt levegő súlyának.
A foszfor elégetésével, végzett egyszerű kísérlet jó példával szolgál Lavoisier mennyiségi vizsgálati módszereinek bemutatására. így végezte ezt a kísérletet (lásd az ábrát): körülbelül hat literes üvegburát oxigénnel töltött meg. A bura higanyba merült, ennek felületére csészét tett, ebbe 61 és 1/4 szemer foszfort. A higany E—-F magasságban állott a burában. Most meggörbített tüzes vassal meggyújtotta a foszfort, ez gyorsan elégett fényes lánggal, erős hőfejlesztéssel. A hirtelen fölmelegedés az első pillanatban erősen megnövelte az oxigén térfogatát és lenyomta a higany színvonalát, de ez hamarosan jóval az előbbi szint fölé emelkedett, amint a foszfor egyesült az oxigénnel. A bura belül csupa fehér pehellyel volt teli. A kísérlet kezdetén 162 köbhüvelyknyi oxigén volt a burában, a kísérlet befejezésekor már csak 23 és 1/4 köbhüvelyknyi, tehát elnyelődött 138 és 3/4 köbhüvelyknyi vagy 69 375 szemernyi. A foszforból megmaradt valamennyi, ami nem égett el, ennek súlya megtisztítás és megszárítás után 16 és 3/4 szemer volt. Tehát 45 szemernyi foszfor égett el, ez egyesült 69 375 szemernyi oxigénnel. A zárt térből semmi nem távozhatott el, üveg és higany akadályozta meg ezt, tehát annak az anyagnak, amely elégéskor fehér pelyhek alakjában keletkezett, egyenlőnek kellett lennie az elégett foszfor és elhasznált oxigén súlyával = 114 375 szemerrel. Így is volt. Persze, ha ma végezzük el ugyanezt a kísérletet, a számszerű eredmények eltérnek. Ennek oka, hogy akkor még nem voltak olyan precíziós mérlegek, a használt vegyi anyagokat sem tudták olyan tisztán előállítani. Lavoisier így foglalja össze ennek a kísérletnek minőségi eredményeit: »A foszfor az elégés következtében, akár közönséges levegőben, akár oxigénben történik ez, pelyhes fehér anyaggá alakul át és egészen új tulajdonságokat vesz föl. Nemcsak vízben oldhatóvá válik, míg azelőtt oldhatatlan volt, hanem meglepő gyorsan magához vonja a levegőben levő nedvességet, és a vízinél sokkal nagyobb fajsúlyú folyadék lesz belőle. Elégése előtt a foszfor majdnem íztelen; oxigénnel való egyesülése után erősen savanyú ízt vesz föl. Végre az éghető anyagok csoportjából átmegy az éghetetlenek közé, és azzá lesz, amit savnak neveznek".
Ami így a foszfor vagy kén elégetésénél keletkezik, az a mai vegytani nyelven foszforsav- vagy kénsavanhidrid, amelyből csak vízfölvétel után lesz sav. Csak későbben jöttek rá, hogy vannak savak, amelyekben nincsen oxigén. Akkor a savfogalom ismét módosuláson ment át, az »oxigén« (savképző) elnevezés is helytelenné vált, mégis megmaradt. De Lavoisier addig is fölfogásának megerősítését látta a salétromsavval végzett kísérleteiben. Lemért mennyiségű higanyt salétromsavban oldott, miközben az a nitrogénoxidgáz fejlődött, amelyet Priestley salétromos levegőnek nevezett. Ha a keletkezett higanynitrátot hevítette, salétromos levegő keletkezett, és vörös higanyoxid maradt vissza, ez megint az izzításnál oxigénre és a kísérlet elején lemért mennyiségű higanyra bomlott fel. Így hát mind az oxigén, mind a salétromos levegő csakis a salétromsavból származhatott. Ez a logikus gondolkodás nagyon jellemző Lavoisierra.
Lavoisier foszfort éget el üvegbura alatt.

Mint mondottuk, Lavoisier központi problémája az égés volt. Amint földerítette az oxidok és savak igazi természetét, megint az égéstüneményekhez fordult. A levegőről Lavoisier mutatta ki, hogy két gázból áll, az oxigénből és nitrogénből, bár ez utóbbit még alig vizsgálták. A vízről is kiderítették, hogy két gáz összetétele. A föld fogalma teljesen megváltozott, egészen mást jelentett, mint az ókorban vagy az alkémistáknál. Csak a tűzzel nem voltak még tisztában. Még mindig sokan tartottak Pliniusszal, aki ezt mondta a tűzről: »A kén nagy mennyiségű tüzet foglal magában. Égésnél ez a tűz kiválik láng és meleg alakjában ugyanakkor, mikor az éghető anyag eltűnik«. Ebben benne van a flogiszton elgondolása is, s ez az, amit Lavoisier gyökerestül felforgatott. Hiszen már a flogisztonban hivő Macquer is ezt mondta: "A nagy elv az, hogy égés nem történhetik szabad levegő hozzájárulása nélkül". Lavoisier klasszikusan vet véget ezeknek a fölfogásoknak a következő tételével (»Sur la combustion en général«, "Az égésről általában"): »A testek csakis levegő, illetve oxigén jelenlétében éghetnek, mert se légüres térben, se másféle gázban nincsen égés. Minden égésnél oxigén tűnik el s az elégett test súlya pontosan annyival nagyobb, mint amennyi oxigént fölvett. Végül minden elégett test savvá változik, amilyen a foszforsav, kénsav, szénsav stb.«
Ebben a meghatározásban persze tévedések vannak, Lavoisier még nem tudta, hogy égés történhetik klór- vagy fluorgázban is, A lényeg az, hogy tisztázta az égés mibenlétét. De foglalkozott a bonyolultabb égés jelenségekkel is, ahol az égés nem csupán a levegő oxigénjével való egyesülésből áll, hanem gáz alakú termékek is keletkeznek. Ilyen például a gyertya és más szerves anyagok égése. Kimutatta, hogy az ilyen égés lényege is az oxigénnel Való egyesülés, de ugyanakkor szénsav is keletkezik. Ha ilyen égés légköri levegőben megy végbe, ennek csak egy része alakul át szénsavvá, a másik része, a nitrogén változatlan marad, míg ha tiszta oxigénben történik az égés, az egész légnemű maradék szénsav. Ezt megint csak bizonyítéknak veszi arra, hogy csupán az oxigén táplálja a tüzet, a nitrogén közömbös gáz.
A levegő összetételének kiderítésével Lavoisier megoldotta az élet egyik legfontosabb közegének titkát. De a másik éltető elemnek: a víznek mibenléte még mindig rejtély volt. Hiába fedezte föl Cavendish a hidrogént már 1767-ben, egy évtizeddel későbben, 1787-ben Macquer még ezt írta:
»A víz meg nem változtatható és föl nem bontható anyagnak látszik; legalábbis mindeddig nem ismeretes egy olyan kísérlet sem, amelyből arra lehetne következtetni, hogy a víz fölbontható.«
Az éghető levegőt, vagyis a hidrogént ismerték, de nem tudták mire magyarázni. Tudták, hogy ha savak hatnak fémekre, ez az éghető levegő keletkezik, de nem tudtak egyebet kezdeni vele, mint hogy megtették valami flogisztonszerű anyagnak, sőt magának a flogisztonnak vélték. Így volt vele a fölfedezője is, Cavendish.
Lavoisier elkezdett foglalkozni a kérdéssel. 1774 márciusában ezt írta laboratóriumi jegyzőkönyvébe: "Meggyőződtem arról, hogy az éghető levegő égése nem más, mint a légköri levegő egy részének fixálódása, a levegő fölbomlása. Ebben az esetben, mint minden levegőben történő égésnél, súlygyarapodásnak kell beállania". A következő év tavaszán fölteszi a kérdést: mi történik, ha az éghető levegő teljesen elég? Itt beleesik elődeinek abba a hibájába, hogy nem tud mindjárt szabadulni valamitől, ami rögeszmévé érlelődött nála, hogy az égésterméknek valami savnak kell lennie, éspedig szénsavnak. De hidrogén elégetése után éppúgy nem talál szénsavat, mint ahogyan Priestley sem talált. 1777-ben hat pint hidrogént éget el egy palackban, amelybe mészvizet is tett. Pedig nemcsak ő figyelte meg, hanem már elődei is, hogy hidrogén elégetésekor víz keletkezik finom cseppek alakjában. De mindenki úgy tekintette ezeket a cseppeket, mint lerakódásokat abból a vízpárából, amely már a kísérlet előtt ott volt a gázokban.
Ekkor már voltak jelentések arról, hogy a hidrogén egyesül az oxigénnel. Priestley már 1774-ben megfigyelte, hogy egy térfogatnyi éghető levegő elégéséhez két térfogatnyi flogisztizált levegő kell. Volta, a villamosságtan nagy elindítója, szintén megfigyelt effélét. A Priestley által többször említett Wartlire angol fizikus zárt és száraz edényben villamos szikrával gyújtotta meg levegő és hidrogén keverékét, s észrevette az edény falához tapadó nedvességet, de nem tudta más magyarázatát adni, mint hogy ez a nedvesség már előzetesen ott volt a gázokban: talán a villamos szikra által okozott flogisztizálás csapta ki. De Cavendish már meglátta a kérdés lényegét: a hidrogén elégetésénél keletkező víz mennyisége sokkal nagyobb, semhogy ezt párák előzetes jelenlétével lehetne magyarázni. De azért még nem vonta le a következtetést, és a kísérletről is csak 1784-ben tett jelentést a londoni Akadémiának.
Ekkor jött Lavoisier. Blagden-től értesült Cavendish kísérleteiről, és rögtön megismételte azokat. Hogy mennyire nem a véletlenre bízta a dolgot, hanem előzetesen jól átgondolt kísérletet végzett, ezt bizonyítja, hogy mindenekelőtt új készüléket szerkesztett meg két nyílással és két gáztartóval. 1783. június 24-én égetett el először hidrogént oxigénben: tekintélyes mennyiségű vizet kapott, minden más termék nélkül, s megállapította, hogy a keletkezett víz súlyának egyenlőnek kell lennie a két elhasználódott gáz súlyával. Több tudós jelenlétében végezte ezt a kísérletet, köztük volt Blagden is, a londoni Akadémia tagja. Már másnap bejelentette az eredményt a francia Akadémiának. Most már megértette azokat a jelenségeket is, amelyek fémeknek savakban való oldásánál mutatkoznak: a víz nem lehet más, mint hidrogén és oxigén vegyülete, a fémek savakban való oldásánál a víz fölbomlik, oxigénje egyesül a fémmel, a hidrogén szabaddá válik. E fölismerés, után rögtön áttért a szintetikus úton való ellenőrzésre, vizet állított elő hidrogénből és oxigénből, sőt a két gáz vegyületi arányát is elég pontosan megállapította. Későbben rájött a víz fölbontásának arra a módjára is, hogy izzó vasdarabok között vezetett át vízgőzt: a víz oxigénje egyesült a vassal, a szabad hidrogén eltávozott. (Némi módosítással ezt a módszert alkalmazzák a gázgyárak még ma is a vízgáz gyártásánál: vízgőzt vezetnek el izzó szén. között, akkor szabad hidrogént és szénoxidot kapnak.)
Így ismerte meg az ember két legfontosabb életelemének, a levegőnek és víznek mibenlétét.
A víz összetételének fölfedezése és a Lavoisier által ebből levont következtetések természetesen véglegesen kihúzták a gyékényt a flogiszton-elmélet lába alól. Sok kiváló vegyész egyenesen megijedt, hogy mi lesz most. Macquer ezt írja 1778. január 1-én: "Lavoisier úr már régóta ijesztget egy nagy fölfedezéssel, amelyet in petto tart és amely alapjában akarja fölfordítani a flogiszton-elméletet; az ő bizakodó arca halálos félelmet olt belém. Hová is jutunk öreg vegytanunkkal, ha egy egészen más épületet kell fölépítenünk? Megvallom önnek, szeretném abbahagyni a játékot. Szerencsére Lavoisier úr éppen közzétette a fölfedezését; megvallom, hogy azóta kisebb súly nyomja a gyomromat... ítélje meg, van-e okom ilyen nagy félelemre".
Csak egy ember van, aki egy pillanatig sem habozik a következmények levonásában, ez maga Lavoisier. Határozottan kimondja:
"Ha minden kielégítően megmagyarázható a vegytanban a flogiszton segítsége nélkül, akkor maga ez a körülmény végtelenül valószínűvé teszi, hogy a princípium nem létezik, csupán alaptalan föltevés. Valóban, a helyes logika elveihez tartozik, hogy ne szaporítsuk fölöslegesen a dolgokat. Talán meg kellett volna maradnom ezeknél a negatív bizonyítékoknál; de ideje, hogy pontosabban és határozottabban nyilatkozzak egy véleményről, amelyet a vegytan szomorú tévedésének tartok és amelyről úgy látom, hogy jelentékenyen feltartóztatta a haladást az általa bevezetett helytelen gondolkodásmóddal."
Majd hozzáteszi:
"A vegyészek bizonytalan és nem rendesen meghatározott principiumot csináltak a flogisztonból, s így aztán mindent megmagyarázhatnak vele, amit akarnak. Ennek a princípiumnak néha van súlya, néha nincs; olykor azonos a szabad tűzzel; olykor a földes elemmel kombinált tűz; olykor áthatol az edények falán, olykor ezek áthatolhatatlanok számára. Egyidejűleg megmagyarázza az anyagok maró vagy nemmaró voltát, átlátszóságát vagy áttetszőségét, a színességet és a színek hiányát: igazi Proteus, amely minden pillanatban változtatja az alakját."
Ennek az érvelésnek alaposságát, egybevetve a tényekkel, hamarosan belátta minden vegyész, elsősorban persze a fiatal nemzedék, amelynek gondolkodása még nem volt olyan mélyen "flogisztizálva". A nagy vegyészek közül Berthollet volt az első, az akadémiának 1785. április 5-én tartott ülésén nyilvánosan Lavoisier mellé állott. Példáját egyenként követi a többi tudós: Morveau 1786-ban, Fourcrov a következő évben, aztán Monge, Meusnier és Chaptal; Laplace már régebben is híve volt.
Lavoisier a fenti vizsgálatokkal indította el a vegytan új korszakát. De más érdemei is vannak ekörül. Miután megállapította az égés mibenlétét, ennek eredményeit alkalmazta a szerves anyagok vizsgálatánál is. Itt is lerakta azt az alapot, amelyen dolgozik még a mai vegytan is. Fentebb már említettük, hogyan magyarázta meg a szénsav keletkezését szerves anyagok (viasz, alkohol, olaj stb.) elégésénél. 1787-ben végezte ezeket a kísérleteket, s akkor észlelte, hogy ilyenkor mindig keletkezik víz is. De mert akkor még nem ismerte a víz vegyi összetételét, nem tudta, hogy ez is összetett test, nem tudta mire magyarázni a keletkezését. De most ilyen szerves anyagokat égetett el tiszta oxigénben, s megállapította, hogy ha ezek teljesen elégnek, csak víz és szénsav keletkezik, semmi más. Akkor tehát ezek a szerves anyagok csakis szénből, oxigénből és hidrogénből állhatnak, a hidrogén és oxigén egyesülnek az elégésnél, s így keletkezik a víz. Ez volt a minőségi megállapítása; de mennyiségi következtetéseket is vont le a tényből: a keletkezett víz és szénsav mennyiségéből következtetni lehet arra, mennyi volt az elégetett anyag szén- és hidrogéntartalma.
Alapvető munkát végzett a biokémia terén is. Sokat foglalkozott a lélegzés vegyi mibenlétével. Erről való megállapításait 1777-ben tette közzé a lélegzés! folyamatról írt dolgozatában. Kimutatta, hogy a lélegzésnél a levegőnek csak egyik alkatrésze használódik föl, az oxigén, amely átalakul szénsavvá és távozik a tüdőből; ez a folyamat szerinte teljesen azonos a szerves anyagok elégésével, tehát ezt kell tekinteni a testmeleg forrásának. Egy Seguin nevű vegyésztársával együtt vizsgálta az izzadás folyamatát is, de kevesebb szerencsével.
Hogy milyen mélyen járó elme volt, az látható abból is, hogy bár nem matematikai formában, de már majdnem kimondotta az anyag megmaradásának elvét. Például ezt mondta: az összetett test súlya egyenlő az alkatrészek súlyával. Mi nagyon magától értődőnek vesszük ezt, de nem így vették abban a korban, amikor a hőt még valami anyagi princípiumnak tartották, mondván, hogy ha vegyi átalakulásoknál hő szabadul föl és távozik el, akkor a keletkezett terméknek könnyebbnek kell lennie, mint amilyen súlyúak voltak az eredeti alkatrészek. Előbb teljesen meg kellett dönteni a flogiszton-elméletet, hogy ez a tétel érvényesülhessen. Íme egy részletes idézet erre vonatkozólag, amit Lavoisier ír az erjedésre vonatkozó kísérleteivel kapcsolatban:
»Semmi nem teremtődik magától se a mesterséges, se a természetes vegyi műveleteknél, és így elvnek vehetjük, hogy minden művelet előtt és után az anyag mennyisége ugyanaz, a princípiumok mennyisége és minősége ugyanaz, csak változások és módosulások történnek. A vegytanban minden kísérlet ezen az elven alapul. Az ember kénytelen föltenni igazi egyenlőséget a vizsgált test princípiumai között és azok között, amelyeket analízis után kapunk.-«
Mi egyéb ez, mint az anyag megmaradásának elve?
Hogy ma a vegytannak nemzetközi nomenklatúrája van, azt is neki köszönhetjük, legalábbis ő vetette meg ennek alapját. Boyle már adott meghatározást az elem fogalmáról: elem az a test, amelyet nem lehet egyszerűbb testekre bontani. Lavoisier is elfogadta ezt a meghatározást. De roppant zavar uralkodott abban a kérdésben, mit tartsanak egyszerű, mit összetett testnek. Hiszen éppen most sült ki két fontos testről, a vízről és levegőről, hogy összetett testek, pedig minden vegyész esküdött volna rá még nemrégen, hogy ezek felbonthatatlanok! Egyszerű testeknek tartották a lúgokat, az ammóniát, a földeket stb., bár ebben már nem voltak olyan bizonyosak.
Most Lavoisier fölfedezte az oxigént, s hirtelenül ez került a kutatások előterébe; sok anyagról kiderült, hogy oxid, s így tarthatatlanná vált a flogisztikusok régi felosztásmódja. Ebben akart rendet teremteni Lavoisier, mikor három kiváló kartársával, Guyton de Morveau-val, Berthollet-ve1 és Fourcroy-val együtt 1787-ben egy munkát adott ki »Méthode de nomenclature chimique« (A vegytani nomenklatúra módszere), címmel. Tulajdonképpen Morveau volt az első, aki fölvetette a nomenklatúra reformjának kérdését. Elemekre és vegyületekre osztják föl a testeket. Az elemek első csoportjába, tartoznak az oxigén, hidrogén és nitrogén, meg Morveau szerint a hő és fény (de Lavoisier nem osztotta ezt a fölfogást). Az elemek második csoportjába tartoznak azok a nemfémek, amelyek savakat képeznek: kén, foszfor, szén s még három föltételezett savgyök: a sósav, a folysav és a bórsav. A harmadik csoportba tartoznak a még föl nem bontott fémek, a negyedikbe a földfémek, az ötödikbe az alkáliföldfémek. Lavoisier azonban annyira nem tartotta elemeknek ez utóbbiakat, hogy »Traité de chimie« című főművében (1789) nem az elemek között sorolja föl őket. Az ekként elfogadott elemeknek aztán vagy a régi nevét tartották meg, vagy a Lavoisier által megkezdett alapon nevezték el őket; oxigén (savképző), hidrogén (vízképző) stb. Erre a kérdésre egyébként még részletesen visszatérünk Berzeliusnál.
2. A VEGYI NOMENKLATÚRA TÖRTÉNETE
Könyvünk ókori és középkori részénél már szóltunk arról, milyen nehéz dolga van a vegytan történetírójának, amikor ezeknek a koroknak vegytani irodalmi termékeit olvassa. Sokszor nem lehet megérteni a szerzőket, mert a mai vegyész nem képes eldönteni, milyen anyagot értett ezer vagy akár ötszáz év előtti elődje ezen vagy azon az elnevezésen. Az anyagelnevezések rendkívül bizonytalanok, nem a test vegyi tulajdonságait kifejezők, mint ma. Például az ókor óta sal (só) néven neveztek mindent, aminek íze sós volt. A VIII. századtól kezdve már valami bizonytalan jelzőt is tettek hozzá, sal maris, sal armoniacum stb. Még Geber-nél sem találunk tudományos elnevezéseket, csak közönséges népieseket, amelyek bizonytalanok. A XIII. században Európában föllépő alkémisták is a népi nevén neveztek mindent; ha mégis valami újat fedeztek föl, ennek legjellemzőbb tulajdonságát jelölték meg az elnevezéssel, például az alkoholt aqua ardens-nek (égő víznek) nevezték. Ha valami közös anyagtulajdonság alapján általánosítottak, ez még rosszabb volt, például egy időben mercurius (higany) néven neveztek mindent, ami illó; a tiszta higany volt a mercurius commun is, az alkohol például mercurius vegetabilis (növényi higany). Még jobban súlyosodott a helyzet, amikor az alkémistákon erőt vett a misztikum iránti hajlam, és képes, metaforikus neveket adtak a vegyi szereknek. Például a szalmiáknak néhány neve: anirna sensibilis (érzékeny lélek), eanoer (rák), aquila (sas), lapis aquilinis (sas-kő), majd angyalokról is nevezték. Ezért nem érti meg a mai vegyész az akkori írásokat, csak más körülményekkel egybevetve tud néha kihámozni valamit.
Ettől kezdve a XVIII. századig inkább a fizikai tulajdonságaik alapján nevezik el a szereket, például akkor oleum volt minden sűrűnfolyó dolog. Viszont sal volt minden, ami vízben oldódott és íze volt: sal tartari, sal nitri stb. Spiritus volt a neve minden illó anyagnak, de sok savnak is. Izük szerint megkülönböztettek salia acida (savanyú sókat) és salia alcalina (lúgos sókat): ha még valami tulajdonságot meg akartak jelölni, még egy jelzőt tettek hozzá: salia alcalina volatilia, illó lúgos sók. Mikor aztán a XVII. századtól kezdve néhány különleges sót fedeztek föl, ezek a fölfedező nevét kapták,, ha a sónak nem volt valami más különös ismertető jele; így keletkeztek ilyen nevek: sal digestivum Sylvii (Sylvius emésztősója), sal minabile Glauberi (Glauber csodálatos sója) stb.
Az alkémia korában csak a legközönségesebb anyagok neve maradt meg, amúgy a fantázia dolgozott vadul az elnevezéseknél, ez is egyik módja volt a fontoskodó titkolódzásnak. Az orvosi vegytan korában is így van még, de a különböző orvosi szerzők mégis ugyanazokkal a szavakkal jelölik a gyakoribb vegyszereket. Csak a XVII. század után lesznek az elnevezések valamivel ésszerűbbek, amennyiben a hasonló tulajdonságú anyagok hasonló neveket kapnak. Például a XV. században Valentinus Basilius még minden kristályos fémsót vitriolnak nevez, a XVIII. századtól kezdve már csak a kénsavas sókat nevezik így; a salétromsavas sókat kezdik salétromnak nevezni, ami izzó szénen elpuffan, az minden salétrom; de a közönséges salétromtól megkülönböztették Glauber lángoló salétromát, az ezüstsalétromot és az ólom,salétromot. Hogy milyen zűrzavaros volt a nomenklatúra ebben az időben, mutatja egy anyagnak, a kénsavas káliumnak egyformán használatos öt neve: sál polychrestum Glaseri, tartarus vitriolatus, vitriolum potassae, sal de duobus,. arcanum duplicatum; némelyiket nem is értjük.
Ez volt a helyzet egészen a XVIII. század végéig, bár már a század közepén voltak törekvések (Macquer, Baumé), hogy a hasonló összetételű anyagokat hasonló nevekkel lássák el, például vitriolok, sók stb. Bergman már alkalmas összetett nevekkel látta el azokat a vegyszereket, amelyeknek összetételét ismerni vélte, de azért még ő is a régi nomenklatúrára támaszkodott, például a lúgokat így különböztette meg: tiszta fix növényi alkáli,, tiszta fix ásványi alkáli, tiszta illó alkáli stb. Csak 1782-től, kezdve használja az egyszerű potassinum, natrum és ammoniacum kifejezéseket. Javaslatot tett
— már Guyton de Morveau értelmében — hogy adjanak valami egyszerű nevet minden savnak, például a salétromossav neve legyen nitreum, a salétromsavé nitrosum; ugyanazon savnak a sói kapjanak vezeték- és keresztnevet, például a kénsavas borkő neve legyen vitriolicum potassinatum. De maga Bergman sem használta következetesen a saját elnevezéseit. Mégis annyira átérezte törekvésének helyes és szükséges voltát, hogy mikor élete utolsó napjaiban értesült Morveau hasonló törekvéseiről, levelet írt neki, s azt tanácsolta, hogy járjon el szigorúan, dobja el az alkalmatlan neveket, ha még olyan régóta használatosak is "akik már járatosak, könnyen meg fogják érteni ezeket, akik még nem járatosak, még könnyebben megértik".
Ekkor lépett fel Guyton de Morveau (1737—1816) a maga reformtörekvéseivel a nomenklatúra terén. Homályosan talán már előbb is megérezte a reform szükségét, de hogy ez hirtelenül követelő erővel tört ki belőle, annak érdekes háttere volt. Ugyanis őt bízták meg az »Encyclopédie méthodique« vegytani címszavainak kidolgozásával. Akkor látta be, hogy lexikális munkát nem lehet végezni határozott nomenklatúra nélkül! Viszont jól tudta, hogy új nomenklutúra nem ér semmit, ha más vegyészek is nem teszik magukévá, új nomenklatúra vagy közkincs lesz, vagy el kell dobni. Ezért 1782-ben tervezetet dolgozott ki, amelyet a »Journ,al de Physique« közölt. Morveau akkor még a flogiszton-elmélet híve volt, tehát az új nomenklatúrát is ezen az alapon dolgozta ki. Ha az olvasó figyelmesen megnézi alábbi táblázatot, amely a sók és alkatrészeik nomenklatúráját adja, látni fogja, hogy ez már alapvetése volt a mai nomenklatúrának. (Az új megnevezéseket francia eredetiben közöljük, mert részben lefordíthatatlanok).
|
Acides: |
Sels: |
Bases: |
|
vitriolique |
vitriols |
phlogistique |
|
nitreux |
ni trés |
calce |
|
arsénical |
arséniates |
barote |
|
boracin |
boraxs |
or |
|
fluorique |
fluors |
argent |
|
citronien |
citrates |
mercure |
|
oxalique |
oxaltes |
cuivre |
|
sébacé |
sébates |
esprit de vin |
A savak közös vezetékneve itt acides (latinul acida), jelzőnek, illetve keresztnévnek hozzátéve a sav eredetét jelző szó. Ez szép és nagyon egyszerű megoldás, mert a bázis adja a vezetéknevet, a sav a keresztnevet, például vitriol d’argent (ezüstszulfát), vitriol de cuivre (rézszulfát), nitre de mercure (higanynitrát) stb., a só neve megjelöli az alkatrészeket is.
Morveau új nomenklatúráját élénk ellenzés fogadta minden oldalon. A flogiszton-elmélet híveinek azért nem tetszett, mert általában nem szívesen láttak semmiféle újítást. Lavoisiernek és követőinek meg nem kellett azért, mert a flogiszton alapján állott, bár éppen nekik igen nagy szükségük volt arra, hogy új kifejezésekkel népszerűsítsék az új rendszert. De közben Morveau megtért, s amikor 1787-ben személyes érintkezésbe került Lavoisier-val, ez rögtön magáévá tette Morveau terveit. Berthollet és Fourcroy is csatlakozott hozzájuk, így a vegytan akkori legkiválóbb francia képviselői együtt voltak ebben a kérdésben. Lavoisier és Morveau együttesen kidolgozták az új nomenklatúra alapelveit, s az előbbi jelentést is tett erről az Akadémiának. Ebben főleg azt a szempontot emelte ki, hogy a test megnevezése lehetőleg mindjárt tájékoztasson a természetéről, általános tulajdonságairól, főleg az egyszerűbb testeknél. Annál inkább szükség van erre, mert a vegytan mind több testet ismer meg, fogalmai állandóan szaporodnak, a sok régi jelentéktelen szó csak megterheli az emlékezőképességet. De csak természetes, hogy ezek a nagy francia vegyészek megtartották a legegyszerűbb testek, a fémek, lúgok és földfémek neveit, de bevezették az új elemek új neveit: hidrogén, oxigén, azot (későbben nitrogén). Mivel a két alkatrészből álló legegyszerűbb vegyületek többnyire savanyú vagy lúgos természetűek, igyekeztek kifejezni az új névvel, hogy melyik csoportba tartozik a vegyület s ezért az alapanyag neve után odatették az »aeide« vagy »oxyd« megjelölést. A savak nevei mellé odatették jelzőnek a »que« végződést, ami aztán átment a latinba is (icum, például innen van az acidum sulfuricium, acidum aceticuro stb. A kevesebb oxigént tartalmazó savakat az »eux« szóvég-jelzővel különböztették meg, például acide sulfureux a kénessav, acide sulfurique a kénsav. Ugyanígy különböztették meg azokat a sókat, amelyekben a savgyök kevesebb oxigént tartalmaz, ezek »ites« végződést kaptak, például nitrites a salétromossavas sók jelzője, nitrates a salétromsavasoké. — A vegyész-olvasó ennyiből is látja, hogy mai nomenklatúránk evvel alapozódott meg. Innen jutottunk el a mai vegyületnevekig, amelyek ugyan sokszor nyelvbicsaklást okoznak, de pontosan megadják a vegyület összetételét és szerkezetét, például dioxidiamidoarzenobenzol (Salvarsan) megmondja, milyen és hány gyökből van összetéve ez a vegyület.
De százötven év előtt még nem tartott ott a vegytan, hogy szükség lett volna erre.
Franciaországban hamarosan általánosán elfogadták a francia vegyészek új nomenklatúráját, azután külföldön is, bár kissé nehezebben. Angliában Black és más kiváló vegyészek magukévá tették, Németországban is sokan. De azért itt egy Wiegleb nevű tekintélyes vegyész még ezt írta 1791-ben: "A francia vegyészeknek az az ötletük támadt, hogy egy egészen új vegytani műnyelvet dolgozzanak ki. De még Franciaországban sem talált általános tetszésre, a külföldiek meg egyhangúan elutasították". Wieglebnek nem volt igaza, pár éven belül már a német vegyészek is az új elnevezéseket használták. Itt említjük meg, hogy egy igen nagy angol vegyésztudós, akiről nemsokára részletesen szó lesz, Humphrey Davy elvi okokból ellenezte az új nomenklatúrát még 1812-ben is, mondván, hogy egy nomenklatúrának nem szabad elméleti fölfogást kifejeznie, mert megtörténhetik, hogy az elméleti fölfogás megváltozik s akkor össze kell omlania a nomenklatúrának is. De a vegytan elméleti alapja nem változott meg többé annyira, hogy az új nomenklatúrát is el kellett volna dobni.